
【Nature】王牌杀手!僵核TCF7L2介导吸烟引起糖尿病的神经机制
众所周知,吸烟有害健康。烟雾中含有焦油、烟碱(又称尼古丁)和一氧化碳,这些化学物质通过不同途径危害身体。其中,烟碱可作用于中枢神经系统,不仅会引起烟瘾[1],还会影响糖代谢平衡,导致血糖水平升高[2],长期吸烟则会增加机体患第二型糖尿病的风险[3]。
 图片来源:PenBay Pilot
图片来源:PenBay Pilot
研究表明,腹侧被盖区(VTA)表达烟碱型胆碱能受体(nicotine acetylcholine receptor, nAChR)的神经元介导烟碱的成瘾性[4],内侧缰核(medial hebanula, mHb)nAChR阳性神经元介导烟碱的厌恶性反应[5]。但是,有关烟碱如何作用于神经系统以破坏机体糖代谢平衡,我们尚未可知。
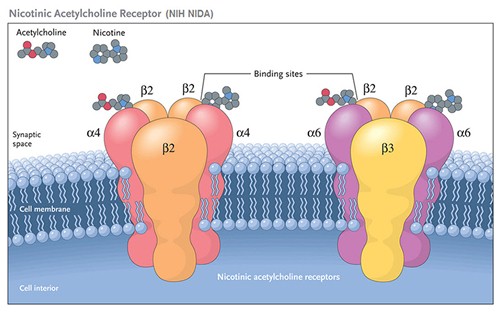 烟碱型胆碱能受体
烟碱型胆碱能受体
近期研究发现,烟碱激活后脑胰高血糖素样肽1(GLP-1)阳性神经元,这些神经元投射到脚间核(IPn)并释放GLP-1,增强mHb在此脑区的兴奋性突触传递[6]。而在胰岛β细胞及很多其他组织中,转录因子TCF7L2是胰高血糖素样肽1(GLP-1)信号通路的核心组分[7],其等位突变与第二型糖尿病密切相关[8],但TCF7L2在脑中的功能依然不明。
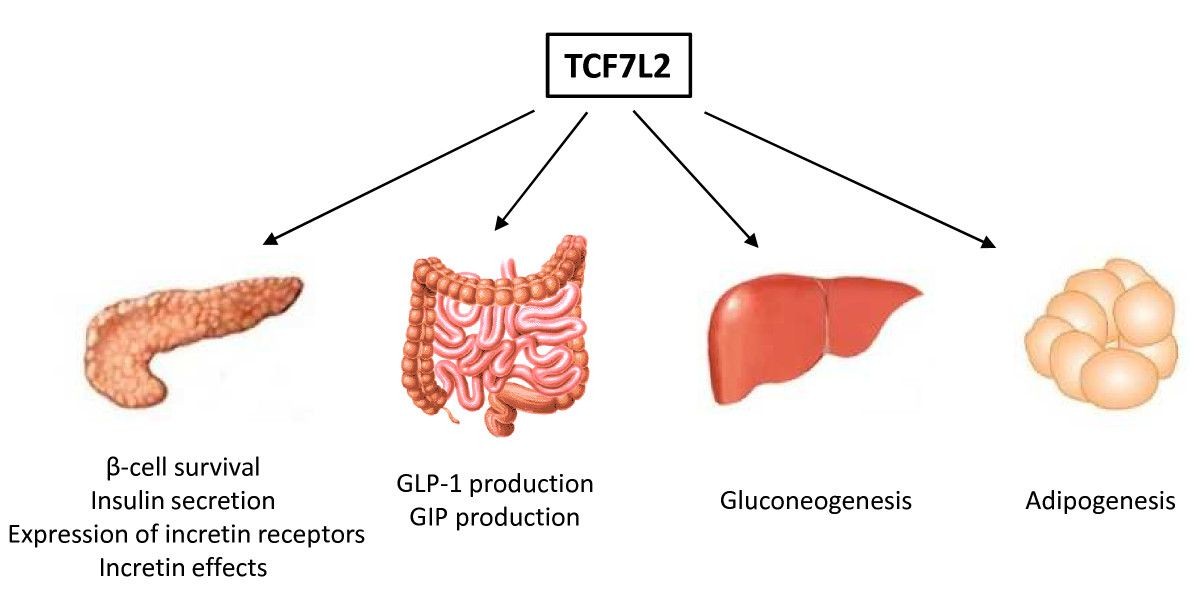 TCF7L2的代谢功能
TCF7L2的代谢功能
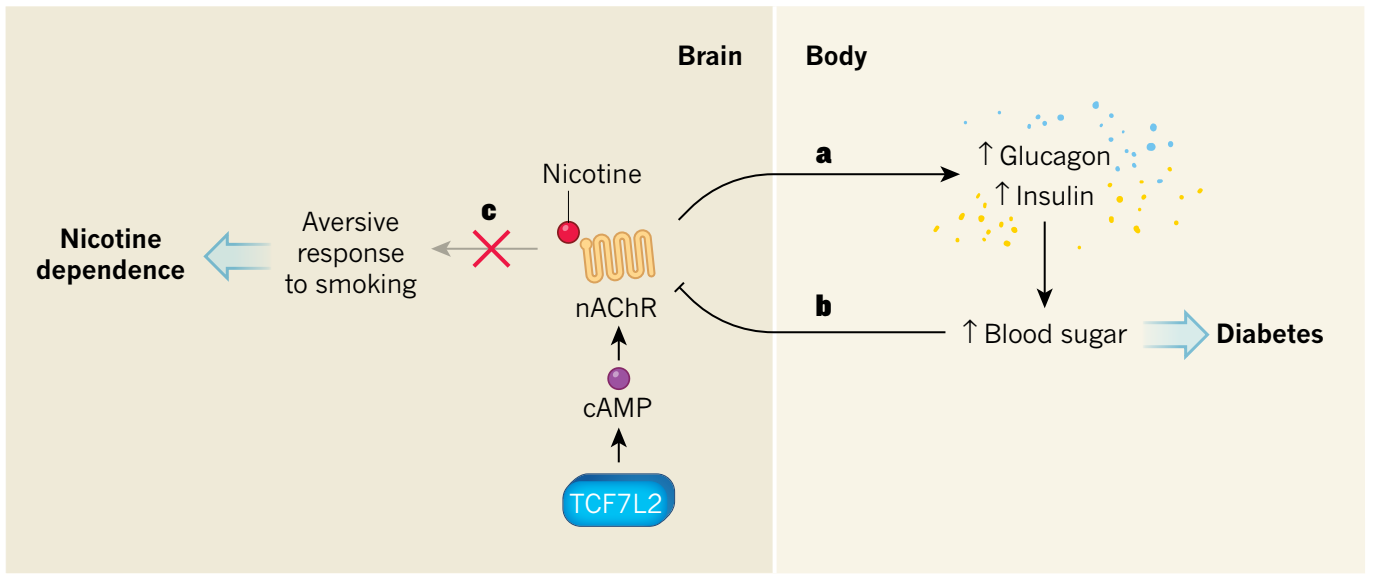
2019年10月17日,《Nature》杂志在线刊登了西奈山伊坎医学院Paul J. Kenny研究组的最新重要工作[10],他们发现TCF7L2在mHb神经元中大量表达,此转录因子通过cAMP通路作用于nAChR,进而介导烟碱升高血糖这一过程。该研究首次揭示TCF7L2在脑中的功能,亦首次发现烟碱引起血糖水平升高的分子、环路机制,极大提高了人们在烟瘾、血糖调节领域的认知。
 Paul J. Kenny, PhD
Paul J. Kenny, PhD
首先,通过翻译核糖体亲和纯化(TRAP)技术,作者发现TCF7L2在 mHb胆碱能神经元中大量表达,而在皮层、海马、纹状体中表达量较低(图1a-e)。然后,作者探究TCF7L2是否调控机体对烟碱的摄取过程。他们引入Tcf7l2突变鼠,发现这种大鼠的烟碱摄取量显著高于正常大鼠,而对食物的摄取量与正常大鼠相似(图1f-i),表明TCF7L2对烟碱摄取的调控作用具有一定特异性。
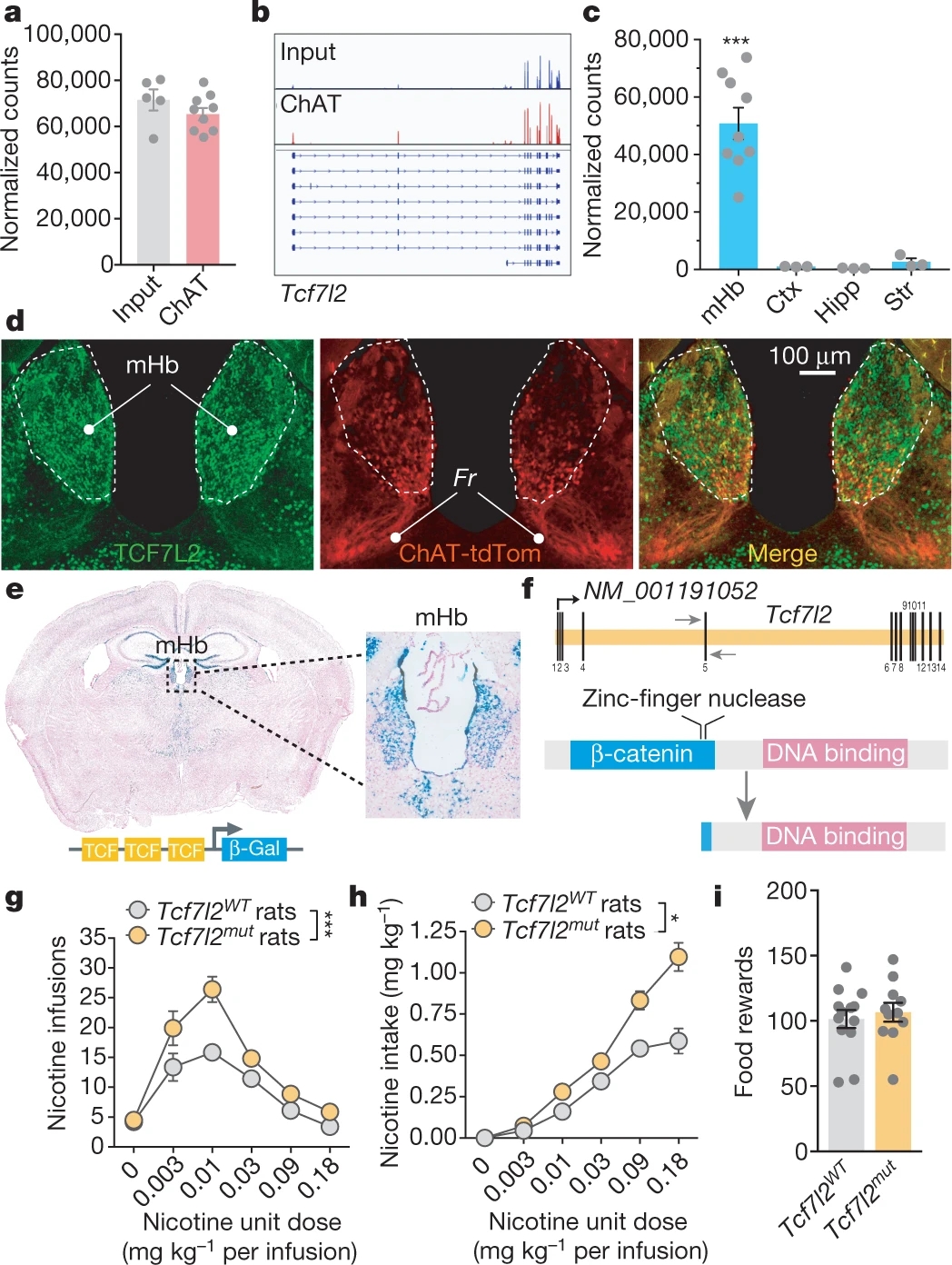 图1 TCF7L2在mHb中大量表达
2.mHb神经元中TCF7L2调控烟碱摄取过程
图1 TCF7L2在mHb中大量表达
2.mHb神经元中TCF7L2调控烟碱摄取过程
前文的方法降低了所有细胞中TCF7L2的表达量,为进一步探究mHb神经元中TCF7L2的功能,作者使用CRISPR-Cas9系统降低TCF7L2表达,他们在spCas9-eGFP小鼠的mHb中注射AAV-Cre和AAV-sgRNA-Tcf7l2,发现这些小鼠的烟碱摄取量显著提高,而食物摄取量不变(图2a-g)。他们还使用了siRNA方法降低mHb神经元中TCF7L2表达,得到相似结果(图2h-k)。以上结果表明,mHb神经元中TCF7L2调控机体对尼古丁的摄取。
为进一步探究上述现象的相关机制,作者使用膜片钳电生理方法记录大鼠mHb神经元。在正常大鼠脑片中,在mHb施加烟碱增加在IPn神经元中记录到的自发兴奋性突触后电流(sEPSC)的频率;而在TCF7L2突变鼠脑片中,在IPn神经元中记录到的sEPSC并不受施加的烟碱影响(图2l-o),表明mHb神经元中TCF7L2可调控烟碱对mHb-IPn环路的激活作用。
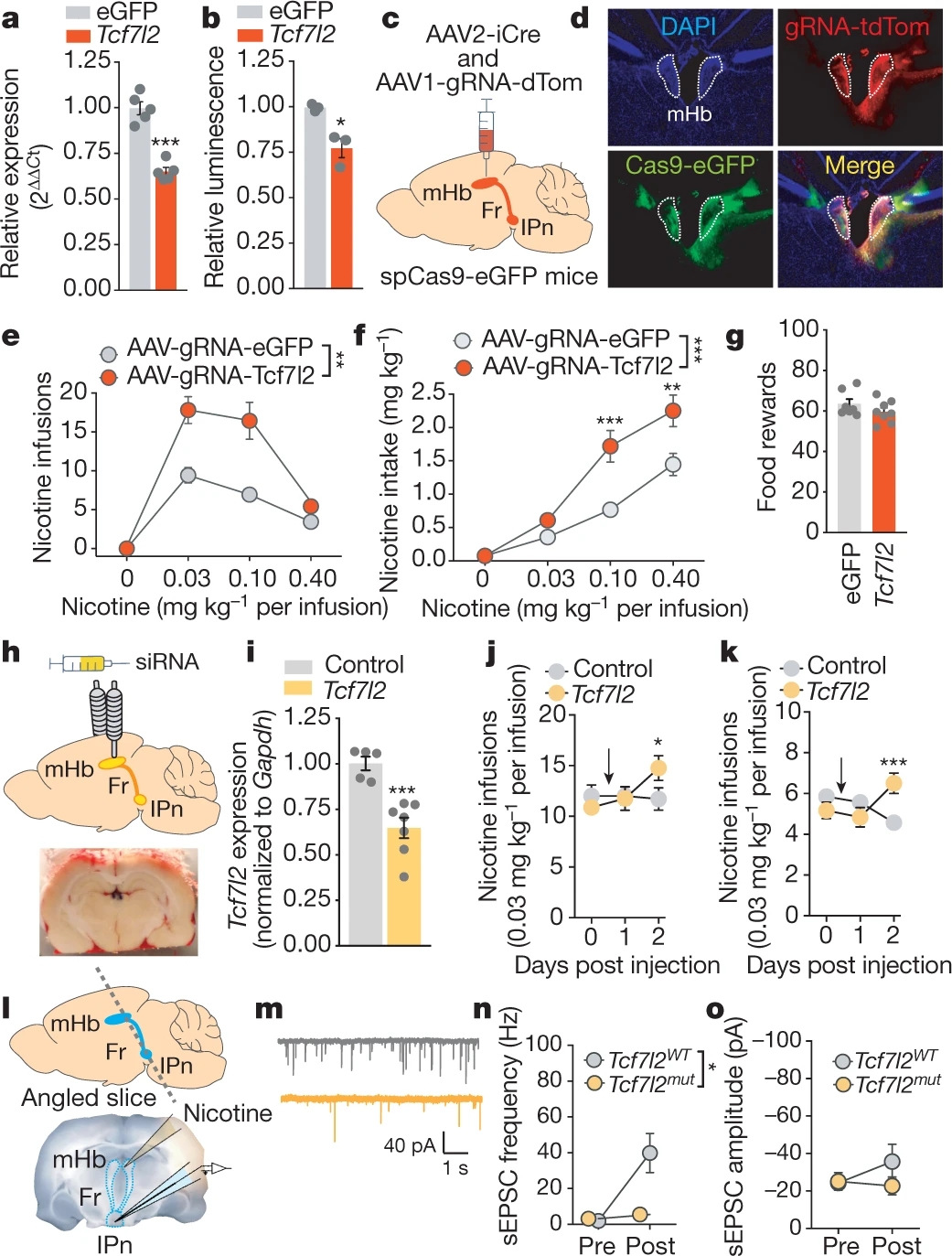 图2 mHb神经元中TCF7L2调控烟碱摄取过程 3.mHb神经元中TCF7L2调控nAChR的功能
图2 mHb神经元中TCF7L2调控烟碱摄取过程 3.mHb神经元中TCF7L2调控nAChR的功能
过去的研究表明,mHb中nAChR阳性神经元介导烟碱的厌恶性反应[5]。为探究mHb神经元中nAChR功能是否受TCF7L2调控,作者使用膜片钳电生理方法记录大鼠mHb神经元,发现在高频施加尼古丁条件下,记录到的nAChR电流的幅度显著减低。而在随后低频施加尼古丁的条件下,正常大鼠mHb神经元中记录到的nAChR电流迅速恢复至本底水平,而TCF7L2突变鼠mHb神经元中记录到的nAChR电流无法完全恢复(图3a-c),表明TCF7L2调控mHb神经元nAChR失敏后的恢复过程。
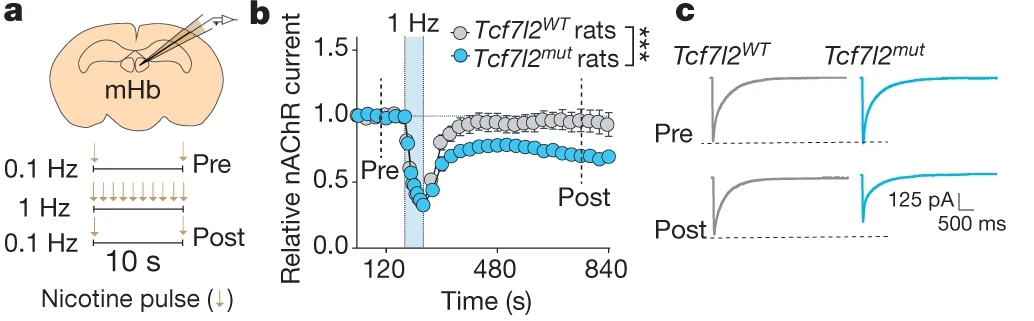 图3 mHb神经元中TCF7L2调控nAChR的功能
4.mHb神经元中TCF7L2调控cAMP信号
图3 mHb神经元中TCF7L2调控nAChR的功能
4.mHb神经元中TCF7L2调控cAMP信号
接下来,作者进一步探究mHb神经元中TCF7L2调控nAChR的分子机制。因为TCF7L2是一种转录因子[11],因此TCF7L2突变鼠mHb神经元中多种基因的表达水平会出现变化,这些基因可能介导TCF7L2对nAChR的调控作用。他们使用RNA测序结合KEGG分析方法探究mHb、 IPn和海马中表达水平显著下调的基因,发现TCF7L2突变鼠mHb神经元cAMP信号显著下调(图4d-f)。
然后,作者通过药理学方法验证上述结论。他们发现,施加EX-4增加正常大鼠而非TCF7L2突变鼠mHb组织中cAMP的表达水平;施加cAMP类似物8-Br-cAMP可恢复TCF7L2突变鼠mHb神经元中nAChR的失敏效应;施加Rolipram增加大脑cAMP表达水平可降低TCF7L2条件敲除鼠的烟碱摄取量(图4h-k)。
以上结果表明,mHb神经元中TCF7L2通过调控cAMP信号进而调节烟碱受体nAChR的功能(图4g)。
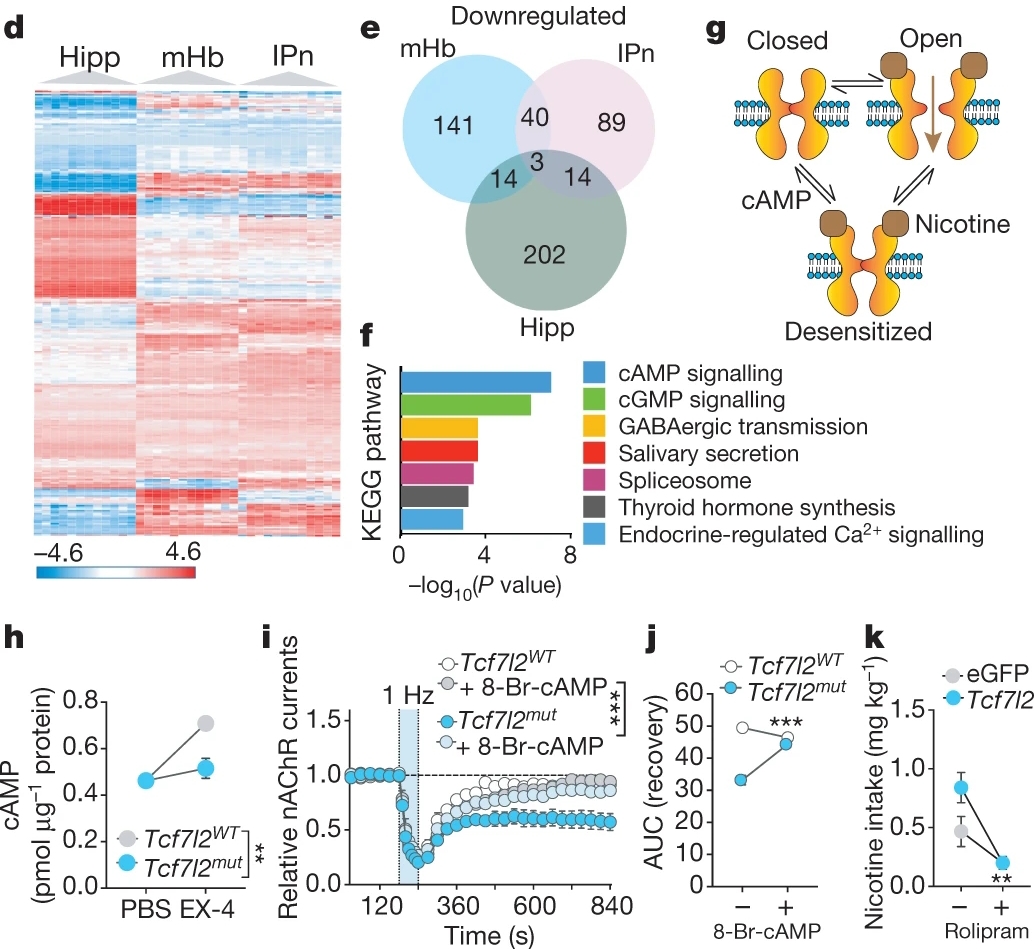 图4 mHb神经元中TCF7L2调控cAMP信号
5.mHb神经元中TCF7L2参与烟碱对血糖水平的调控过程
图4 mHb神经元中TCF7L2调控cAMP信号
5.mHb神经元中TCF7L2参与烟碱对血糖水平的调控过程
鉴于烟碱增加吸烟者的血糖水平[2],吸烟者患第二型糖尿病的风险更高[3],以及TCF7L2等位基因与第二型糖尿病密切相关[8],作者推测mHb神经元中TCF7L2可能会参与烟碱对血糖水平的调控作用。为证实此推测,作者展开以下研究。
他们发现,摄入高浓度烟碱增加大鼠血糖水平,而摄入低浓度烟碱则不会(图5a-c)。然后,他们在大鼠IPn中注射逆行表达病毒AAV-retro-Cre,在mHb中注射AAV-DIO-hM3Dq,发现激活投射到IPn的mHb神经元显著增加大鼠血糖水平,与摄入高浓度烟碱的效应相似(图5d-f)。他们还发现,在mHb中注射EX-4后,低浓度烟碱亦可增加大鼠血糖水平;通过shRNA降低mHb中GLP-1受体的表达水平后,或通过siRNA降低mHb中TCF7L2的表达水平后,抑或腹腔注射无法通过血脑屏障的Atenolol后,烟碱不再增加大鼠血糖水平(图5g-j)。此外,在胰腺中注射pRV-GFP以跨多级逆行示踪支配胰腺的神经元,发现mHb和IPn中均有GFP阳性神经元(图5k-l)。
以上结果表明,烟碱通过作用于mHb-IPn环路以调控胰腺对血糖水平的调节,此过程依赖于GLP-1和TCF7L2。
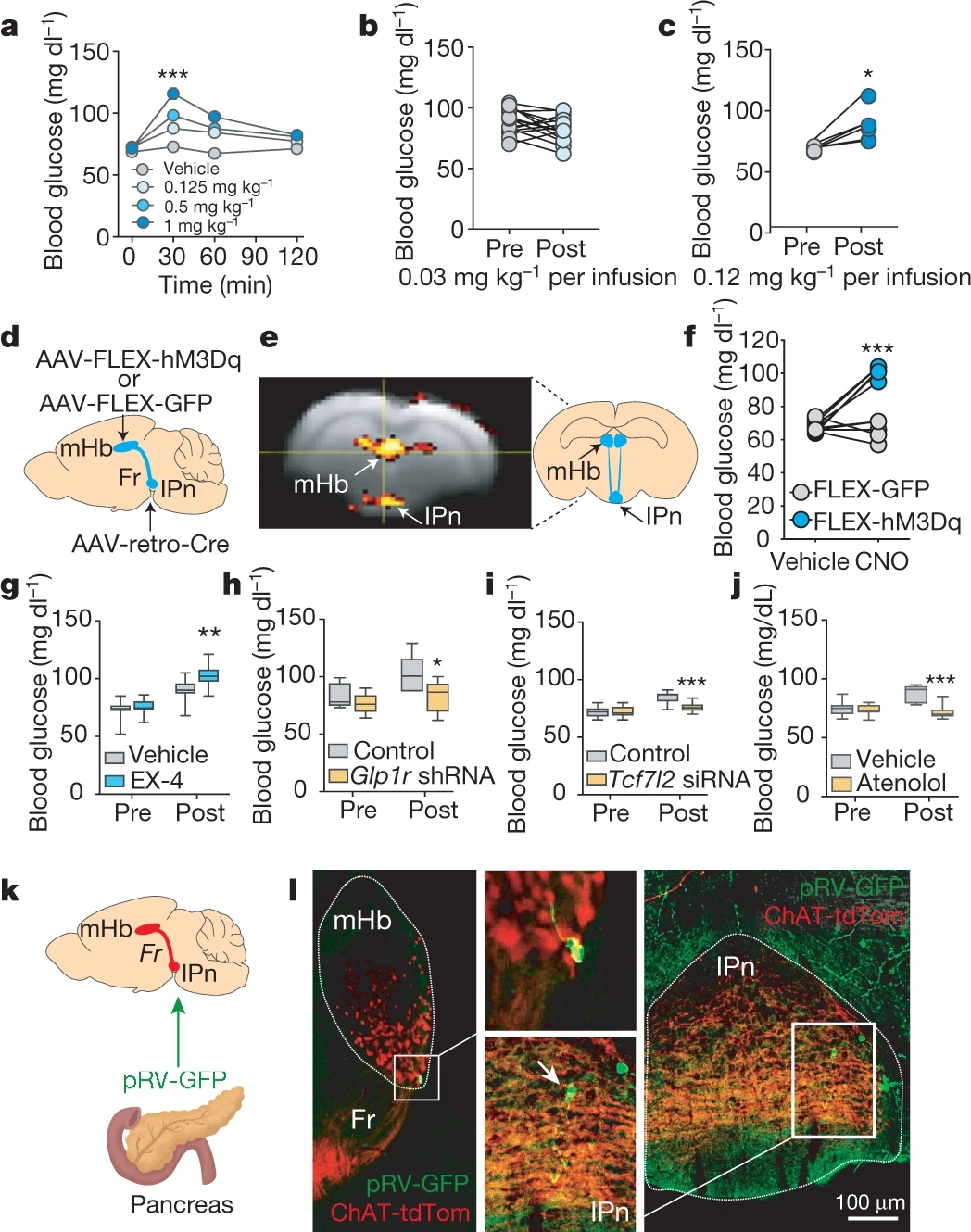 图5 mHb神经元中TCF7L2参与烟碱对血糖水平的调控过程 6.TCF7L2调控烟碱长期作用对机体血糖水平的影响
图5 mHb神经元中TCF7L2参与烟碱对血糖水平的调控过程 6.TCF7L2调控烟碱长期作用对机体血糖水平的影响
最后,作者探究血糖水平对烟碱摄取的反作用。作者让大鼠长期(连续3周)摄入烟碱以模拟长期吸烟的烟民,发现长期摄入烟碱的大鼠的空腹血糖水平显著升高(图6a-c),胰岛素和胰高血糖素的释放量亦显著增加(图6d-e),此效应在烟碱戒断后可维持1个月之久(图6f-h)。而对于TCF7L2突变鼠,长期摄入烟碱反而降低胰岛素和胰高血糖素的释放水平(图6i-k),可能由TCF7L2突变导致机体血糖调控的内稳态失衡所致。
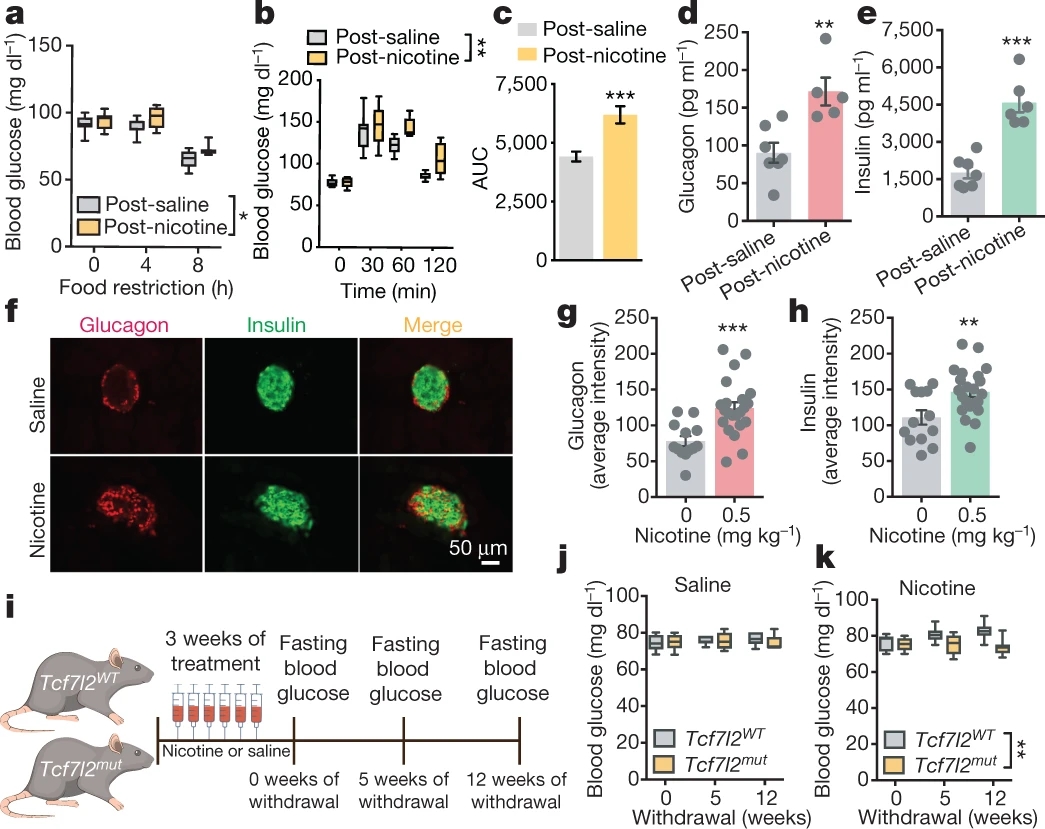 图6 TCF7L2调控烟碱长期作用对机体血糖水平的影响
图6 TCF7L2调控烟碱长期作用对机体血糖水平的影响
长期吸烟的烟民患第二型糖尿病的概率远高于不吸烟的人,但其相关机制尚未可知。本篇文章结合病毒注射、基因编辑、RNA测序、化学遗传学、血糖检测等多种方法,发现mHb神经元中TCF7L2通过cAMP调控nAChR的活性,从而调控mHb-IPn环路功能,进而介导烟碱对血糖水平的调节作用。这项研究阐释了烟碱升高机体血糖水平的分子、环路机制,揭示了长期吸烟者患第二型糖尿病概率更高的诱因,也让我们更加理解——吸烟有害健康!
和元生物 一直关注神经科学领域的重大研究进展,为神经生理、病理研究提供最新工具和研究方案,助力临床转化和基因治疗!
参考文献
1.Stolerman, I.P. and M.J. Jarvis, The Scientific Case That Nicotine Is Addictive. Psychopharmacology, 1995. 117(1): p. 2-10.
2.Haggard, H.W. and L.A. Greenberg, The effects of cigarette smoking upon the blood sugar. Science, 1934. 79(2047): p. 274-274.
3.Willi, C., et al., Active smoking and the risk of type 2 diabetes: a systematic review and meta-analysis. JAMA, 2007. 298(22): p. 2654-64.
4.Maskos, U., et al., Nicotine reinforcement and cognition restored by targeted expression of nicotinic receptors. Nature, 2005. 436(7047): p. 103-7.
5.Benowitz, N.L., Nicotine addiction. N Engl J Med, 2010. 362(24): p. 2295-303.
6.Tuesta, L.M., et al., GLP-1 acts on habenular avoidance circuits to control nicotine intake. Nat Neurosci, 2017. 20(5): p. 708-716.
7.Liu, Z. and J.F. Habener, Glucagon-like peptide-1 activation of TCF7L2-dependent Wnt signaling enhances pancreatic beta cell proliferation. J Biol Chem, 2008. 283(13): p. 8723-35.
8.Fuchsberger, C., et al., The genetic architecture of type 2 diabetes. Nature, 2016. 536(7614): p. 41-47.
9.Ip, W., Y.T. Chiang, and T. Jin, The involvement of the wnt signaling pathway and TCF7L2 in diabetes mellitus: The current understanding, dispute, and perspective. Cell Biosci, 2012. 2(1): p. 28.
10.Duncan, A., et al., Habenular TCF7L2 links nicotine addiction to diabetes. Nature, 2019. 574(7778): p. 372-377.
11.Murray, K.D., P.V. Choudary, and E.G. Jones, Nucleus- and cell-specific gene expression in monkey thalamus. Proc Natl Acad Sci U S A, 2007. 104(6): p. 1989-94.

扫一扫,反馈当前页面
和元生物