上篇文章中,我们简单介绍了新型冠状病毒的基本结构特征,针对国内外临床治疗现状进行了简单梳理(详情点击)。本篇文章,我们将继续介绍针对新型冠状病毒包膜蛋白的结构特征,基因疫苗的临床研发思路有哪些,以及目前国内外基因疫苗的研发现状。
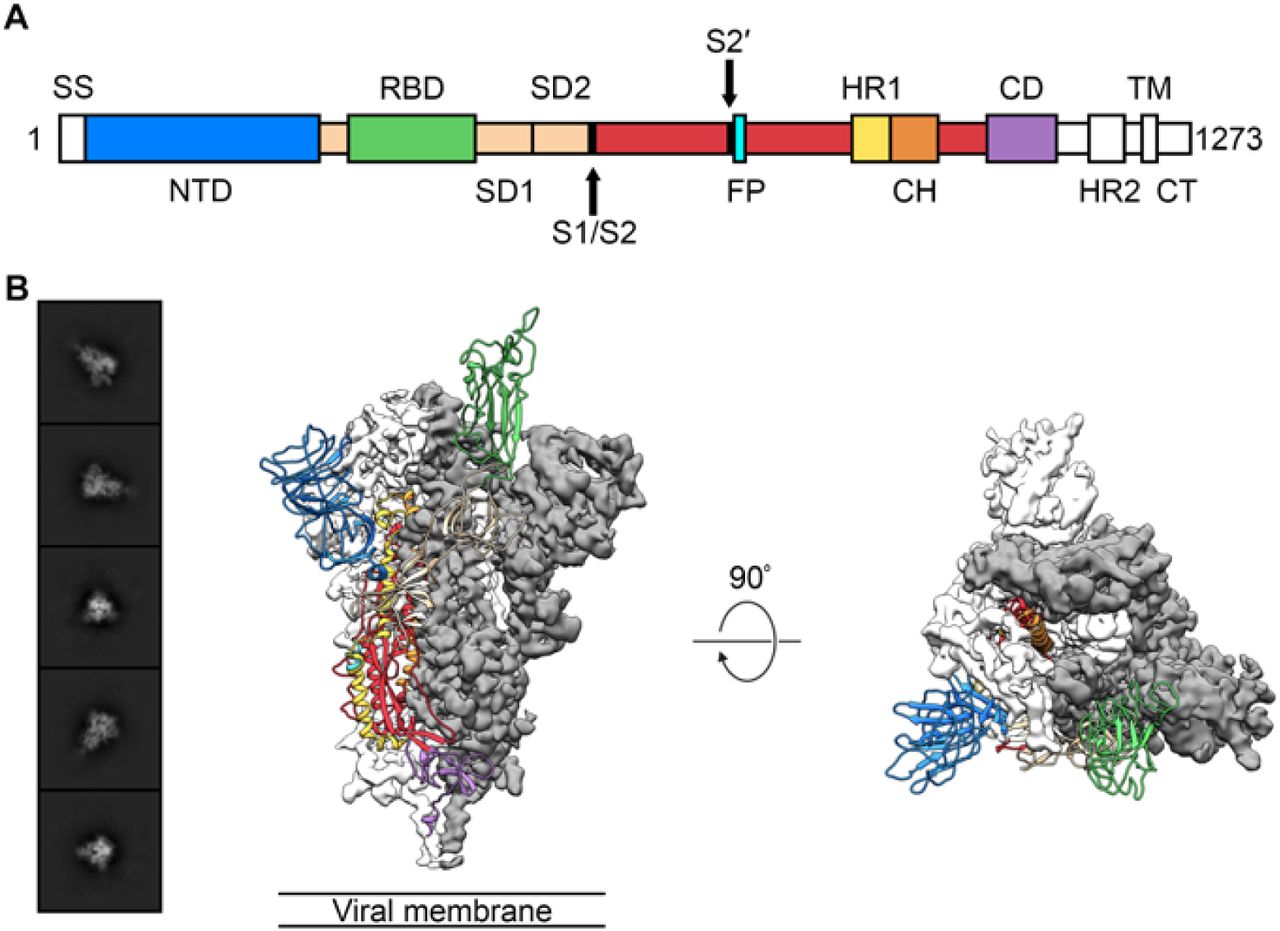
2019-nCoV包膜S蛋白结构
图片来源:puntomagazine; Science, doi: 10.1126/science.abb2507
1.基因疫苗的临床研发思路解析
研究数据表明,2019-nCoV是一种来自Sarbecovirus亚属的新型β冠状病毒,与SARS-CoV同源性为79%,与MERS-CoV同源性为50%。分子建模结果显示,2019-nCoV 与SARS-CoV存在380个差异性氨基酸位点,二者之间的受体结合域类似,尽管存在氨基酸的突变,但2019-nCoV仍通过包膜S蛋白与受体细胞表面ACE2结合而感染宿主细胞[1,2]。
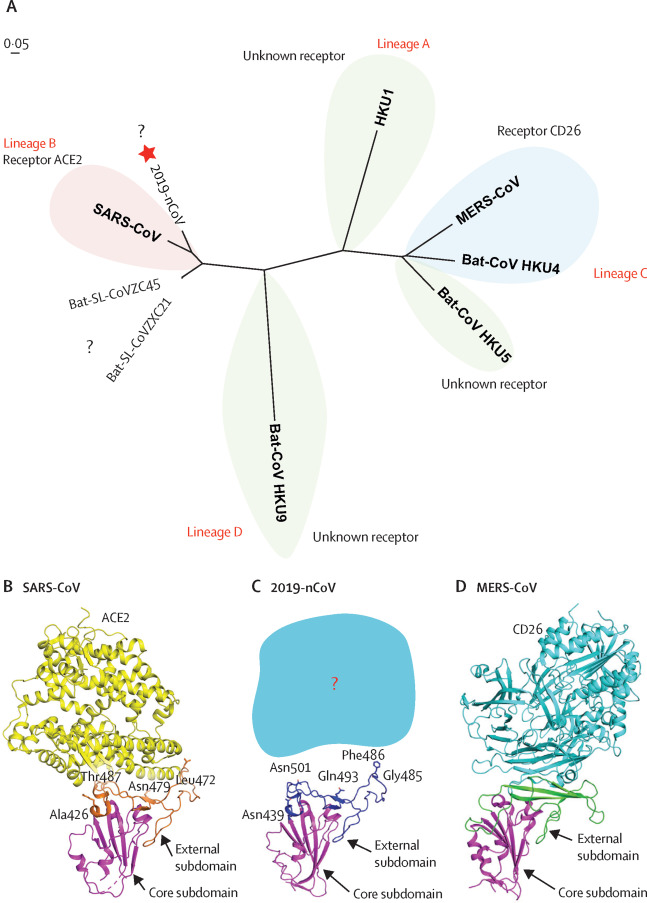
2019-nCoV与SARS-CoV和MERS-CoV受体结合区域(RBD)同源性分析
图片来源:Lancet, 395 (10224), 565-574
因此,我们可以考虑借鉴SARS-CoV和MERS-CoV疫苗研发靶点和思路,应用到2019-nCoV的疫苗研发中。
针对SARS-CoV的基因疫苗主要基于其包膜S蛋白,主要包括DNA疫苗、病毒载体疫苗和mRNA疫苗。
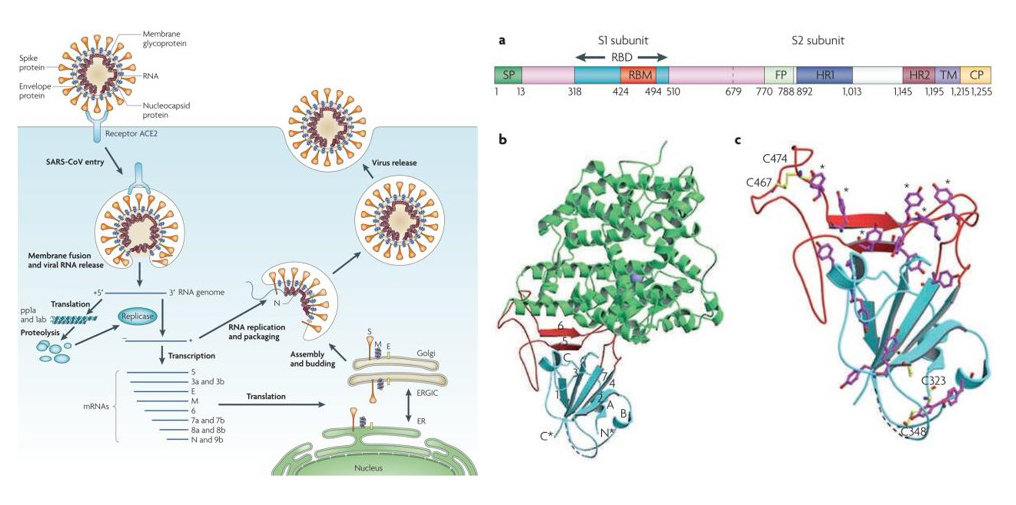
SARS-CoV感染宿主细胞过程及其包膜S蛋白结构
图片来源:Du, Lanying et al. Nature reviews. Microbiology vol. 7,3 (2009): 226-36.
基于SARS-CoV S蛋白研发的DNA疫苗结构简单,易于操作,能够刺激机体产生IgG中和抗体,引起细胞免疫反应;但在人体可能具有低免疫源性,而反复接种又会引起毒性等[5,6]。运用病毒载体制备的疫苗病毒工具包括腺病毒载体、改良型痘苗病毒安卡拉株(MVA)等,病毒载体疫苗能够有效地产生中和抗体和引起细胞免疫,却容易引起ADE[7,8,9]。详见表1。
表1 基于SARS-CoV S蛋白设计的疫苗情况
针对MERS-CoV的基因疫苗主要基于其包膜S全长蛋白、S蛋白三聚体、S蛋白不同亚基及功能单位,主要包括病毒载体疫苗(ADV/MVA/MV/VSV/RABV)、DNA疫苗和mRNA疫苗等,详见下表2,3。
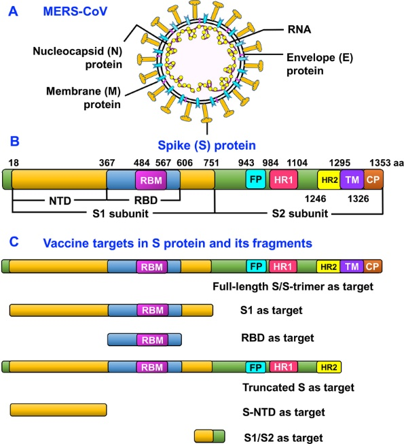
MERS-CoV及其S蛋白结构
图片来源:Expert Rev Vaccines. 2018 August ; 17(8): 677–686.
表2 基于MERS-CoV 全长S蛋白及三聚体结构设计的疫苗情况
表3 基于MERS-CoV 全长S蛋白片段设计的疫苗情况
2.国内外基因疫苗的研发现状
综上所述,我们发现,可通过冠状病毒S蛋白的全长蛋白、片段、不同结构构象或亚基等作为靶点进行疫苗的研发。
而现阶段,对于临床前新冠病毒基因疫苗的研究之所以如火如荼,一是因为疫情爆发,传统抗病毒新药和传统疫苗的研发周期过长,无法赶上快速蔓延的新冠疫情;二是因为传统疫苗(如灭活疫苗和减毒疫苗)对于新冠病毒的有效性和安全性仍存质疑。
因此,突发疫情下,新型疫苗成为扼制疫情蔓延的希望:
Inovio公司与艾棣维欣开发针对新冠病毒的INO-4800DNA疫苗,双方此次合作旨在利用艾棣维欣的技术在中国进行一期试验。Inovio近期宣布,流行病防范创新联盟(CEPI)已经向Inovio提供高达900万美元的资助,以此支持Inovio在美国通过INO-4800一期人体试验,以此评估疫苗的安全性和免疫原性。
康泰与艾棣维欣合作,双方将组成工作小组,协调各方资源,研究开发新冠病毒 DNA 疫苗,解决疫苗临床前研究、临床申报和临床试验中遇到的问题,以加快推进新冠 DNA 疫苗的研发。
康希诺研发的腺病毒载体疫苗目前处于临床前阶段,康希诺公司产品Ad5-EBOV曾在短时间获批上市并成为中国唯一申请用作应急使用及国家储备的埃博拉病毒疫苗。
Johnson&Johnson继续利用AdVac®腺病毒载体平台和/或PER.C6®生产细胞系技术,研发新冠病毒腺病毒载体疫苗,其早前应用该平台开发的埃博拉疫苗目前正在测试阶段。
武汉博沃与GeoVax-BravoVax合作开发新型冠状病毒疫苗,GeoVax Labs将利用其MVA-VLP疫苗平台及专业知识,使用源自武汉的冠状病毒基因序列来设计和构建候选疫苗。
ModernaTherapeutics公司开发的治疗新型冠状病毒的mRNA疫苗mRNA-1273,是针对新冠病毒表面S蛋白而制成的,目前已开始招募健康志愿者,计划于4月底开始正式启东临床。
同济大学附属东方医院转化医学平台与斯微生物科技有限公司合作,依托“上海张江国家自主创新示范区干细胞战略库与干细胞技术临床转化平台”课题子任务——mRNA合成平台成果,快速推动新型冠状病毒mRNA疫苗研发。
目前,和元生物 联合军事医学研究院研发的针对新冠病毒的小试DNA疫苗正在开展动物实验,助力新冠疫情DNA疫苗的快速研发,期望能以实际行动助力国家扼制疫情。
和元生物 近日完成亿元B+轮融资,近7万平米的基因药GMP生产基地已破土动工。CDMO平台可提供临床级重组病毒载体服务,推进基因治疗药物及基因工程疫苗领域,助力基因治疗造福人类的伟大愿景。
更多疫苗相关信息,请您关注和元生物 公众号“obio GeneTherapy”,后续为您分享更多市场和工艺开发信息。
参考文献:
1.Roujian Lu et al., Genomic Characterisation and Epidemiology of 2019 Novel Coronavirus: Implications for Virus Origins and Receptor Binding. Lancet, 395 (10224), 565-574, 2020 Feb 22. DOI: 10.1016/S0140-6736(20)30251-8.
2.Yusen Zhou et al., Prospects for a MERS-CoV spike vaccine. Expert Rev Vaccines. 2018 August; 17(8): 677-686. Doi: 10.1080/14760584.2018.1506702.
3.Czub M, Weingartl H, Czub S, He R, Cao J. Evaluation of modified vaccinia virus Ankara based recombinant SARS vaccine in ferrets. Vaccine. 2005;23:2273–2279.
4.Weingartl H, et al. Immunization with modified vaccinia virus Ankara-based recombinant vaccine against severe acute respiratory syndrome is associated with enhanced hepatitis in ferrets. J. Virol. 2004;78:12672–12676.
5.Yang ZY, et al. A DNA vaccine induces SARS coronavirus neutralization and protective immunity in mice. Nature. 2004;428:561–564.
6.Zhao P, et al. DNA vaccine of SARS-CoV S gene induces antibody response in mice. Acta Biochim. Biophys. Sin. (Shanghai) 2004;36:37–41.
7.Bisht H, et al. Severe acute respiratory syndrome coronavirus spike protein expressed by attenuated vaccinia virus protectively immunizes mice. Proc. Natl Acad. Sci. USA. 2004;101:6641–6646.
8.Chen Z, et al. Recombinant modified vaccinia virus Ankara expressing the spike glycoprotein of severe acute respiratory syndrome coronavirus induces protective neutralizing antibodies primarily targeting the receptor binding region. J. Virol. 2005;79:2678–2688.
9.Kim E, Okada K, Kenniston T, et al. Immunogenicity of an adenoviral-based Middle East respiratory syndrome coronavirus vaccine in BALB/c mice. Vaccine 2014;32(45):5975–82.
10.Munster VJ, Wells D, Lambe T, et al. Protective efficacy of a novel simian adenovirus vaccine against lethal MERS-CoV challenge in a transgenic human DPP4 mouse model. NPJ Vaccines 2017;2:28.
11.Haagmans BL, van den Brand JM, Raj VS, et al. An orthopoxvirus-based vaccine reduces virus excretion after MERS-CoV infection in dromedary camels. Science 2016;351(6268):77–81. A report about a modified vaccinia virus Ankara (MVA) vectored vaccine with protective efficacy against MERS-CoV and camelpox virus in dromedary camels.
12.Volz A, Kupke A, Song F, et al. Protective efficacy of recombinant modified vaccinia virus Ankara (MVA) delivering Middle East respiratory syndrome coronavirus spike glycoprotein. J Virol 2015;89(16):8651–6.
13.Alharbi NK, Padron-Regalado E, Thompson CP, et al. ChAdOx1 and MVA based vaccine candidates against MERS-CoV elicit neutralising antibodies and cellular immune responses in mice. Vaccine 2017;35(30):3780–8.
14.Song F, Fux R, Provacia LB, et al. Middle East respiratory syndrome coronavirus spike protein delivered by modified vaccinia virus Ankara efficiently induces virus-neutralizing antibodies. J Virol 2013;87(21):11950–4.
15.Malczyk AH, Kupke A, Prufer S, et al. A highly immunogenic and protective Middle East respiratory syndrome coronavirus vaccine based on a recombinant Measles virus vaccine platform. J Virol 2015;89(22):11654–67.
16.Liu R, Wang J, Shao Y, et al. A recombinant VSV-vectored MERS-CoV vaccine induces neutralizing antibody and T cell responses in rhesus monkeys after single dose immunization. Antiviral Res 2018;150:30–8.
17.Al-Amri SS, Abbas AT, Siddiq LA, et al. Immunogenicity of candidate MERS-CoV DNA vaccines based on the spike protein. Sci Rep 2017;7:44875.
18.Muthumani K, Falzarano D, Reuschel EL, et al. A synthetic consensus anti-spike protein DNA vaccine induces protective immunity against Middle East respiratory syndrome coronavirus in nonhuman primates. Sci Transl Med 2015;7(301):301ra132.
19.Phase I, Open label dose ranging safety study of GLS-5300 in healthy volunteers. [cited July 27, 2016]. Available from: https://clinicaltrials.gov/ct2/show/NCT02670187?cond=MERS&rank=21.
20.Wang L, Shi W, Joyce MG, et al. Evaluation of candidate vaccine approaches for MERS-CoV. Nat Commun 2015;6:7712.
21.Wang C, Zheng X, Gai W, et al. MERS-CoV virus-like particles produced in insect cells induce specific humoural and cellular imminity in rhesus macaques. Oncotarget 2017;8(8):12686–94.
22.Wirblich C, Coleman CM, Kurup D, et al. One-Health: a safe, efficient, dual-use vaccine for humans and animals against Middle East respiratory syndrome coronavirus and Rabies virus. J Virol 2017;91(2).
23.Chi H, Zheng X, Wang X, et al. DNA vaccine encoding Middle East respiratory syndrome coronavirus S1 protein induces protective immune responses in mice. Vaccine 2017;35(16):2069–75.
24.Wang C, Zheng X, Gai W, et al. Novel chimeric virus-like particles vaccine displaying MERS-CoV receptor-binding domain induce specific humoral and cellular immune response in mice. Antiviral Res 2017;140:55–61.
25.Mou H, Raj VS, van Kuppeveld FJ, et al. The receptor binding domain of the new MERS coronavirus maps to a 231-residue region in the spike protein that efficiently elicits neutralizing antibodies. J Virol 2013;87(16):9379–83.