
王红阳院士团队揭示NAD+代谢调节肿瘤免疫逃逸和增强PD-1/PD-L1治疗敏感性
烟酰胺腺嘌呤二核苷酸(NAD+)是能量代谢和信号转导途径的重要中介[1],除了在氧化磷酸化和氧化还原反应中的功能外,NAD+还作为许多酶的底物,并参与许多生物过程,如DNA修复、炎症和蛋白质乙酰化[2]。烟酰胺磷酸核糖基转移酶(NAMPT)是NAD+合成途径的限速酶,NAMPT和NAD+在几种人类恶性肿瘤中经常上调,并在肿瘤的起始、进展和复发中发挥关键作用[3]。然而,NAMPT介导的NAD+代谢在调控肿瘤免疫逃逸中的作用尚不清楚。
近年来,免疫检查点抑制剂在肿瘤免疫治疗方面取得了显著的临床突破。程序性死亡配体1(PD-L1,也称为CD274或B7-H1)在多种癌症中高表达,并通过与活化的T细胞表面的受体PD-1相互作用来调节免疫逃逸,导致T细胞衰竭。PD-1/PD-L1轴抑制剂可显著增强T细胞应答,并在多种晚期癌症中表现出显著的临床应答。
然而,临床试验数据显示,抗PD-1/PD-L1抗体等免疫治疗在实体瘤中的有效率低,仅20%左右。此外,长时间持续性的单一使用免疫检查点抑制剂治疗肿瘤并不能收到预期的疗效,甚至容易引发免疫耐受。因此,寻找行之有效的疗效预测标志和联合治疗是提高肿瘤免疫治疗效果和推进肿瘤精准免疫治疗的重要方法。NAD+代谢与癌症有关。然而,其在免疫检查点调控和免疫逃逸中的作用尚不清楚。
第二军医大学东方肝胆外科医院/国家肝癌科学中心王红阳院士/杨文研究员团队在Cell Metabolism上发表了题为 NAD+ metabolism maintains inducible PD-L1 expression to drive tumor immune evasion 的研究论文,揭示了NAD+代谢通过调节免疫检查点PD-L1的表达,驱动肿瘤免疫逃逸的新机制,并提出了通过补充NAD+前体增强免疫治疗耐受肿瘤对抗PD-1/PD-L1抗体治疗敏感性的新策略[5]。

结果
1 NAD+代谢控制CD8+T细胞依赖性肿瘤抑制作用
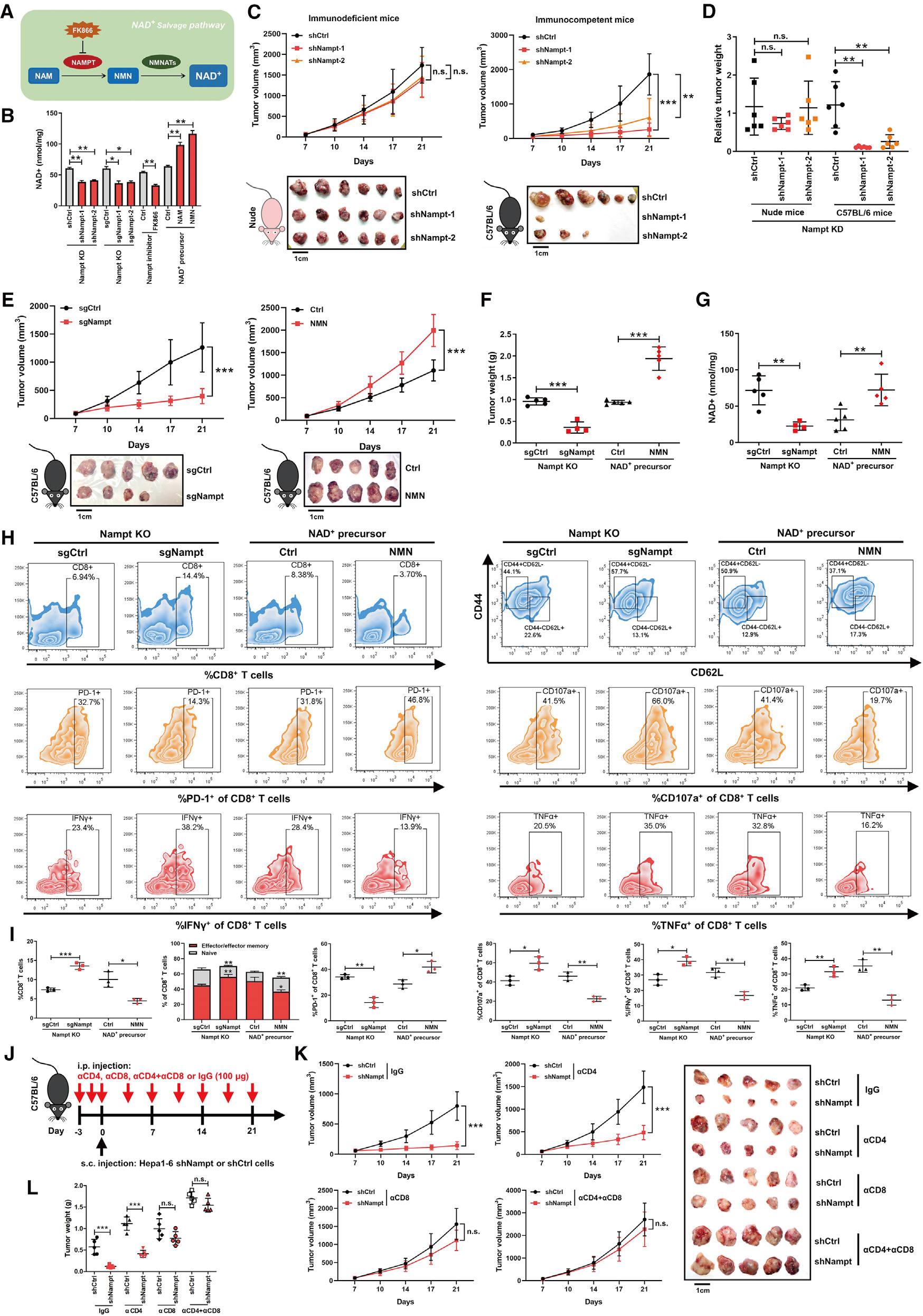
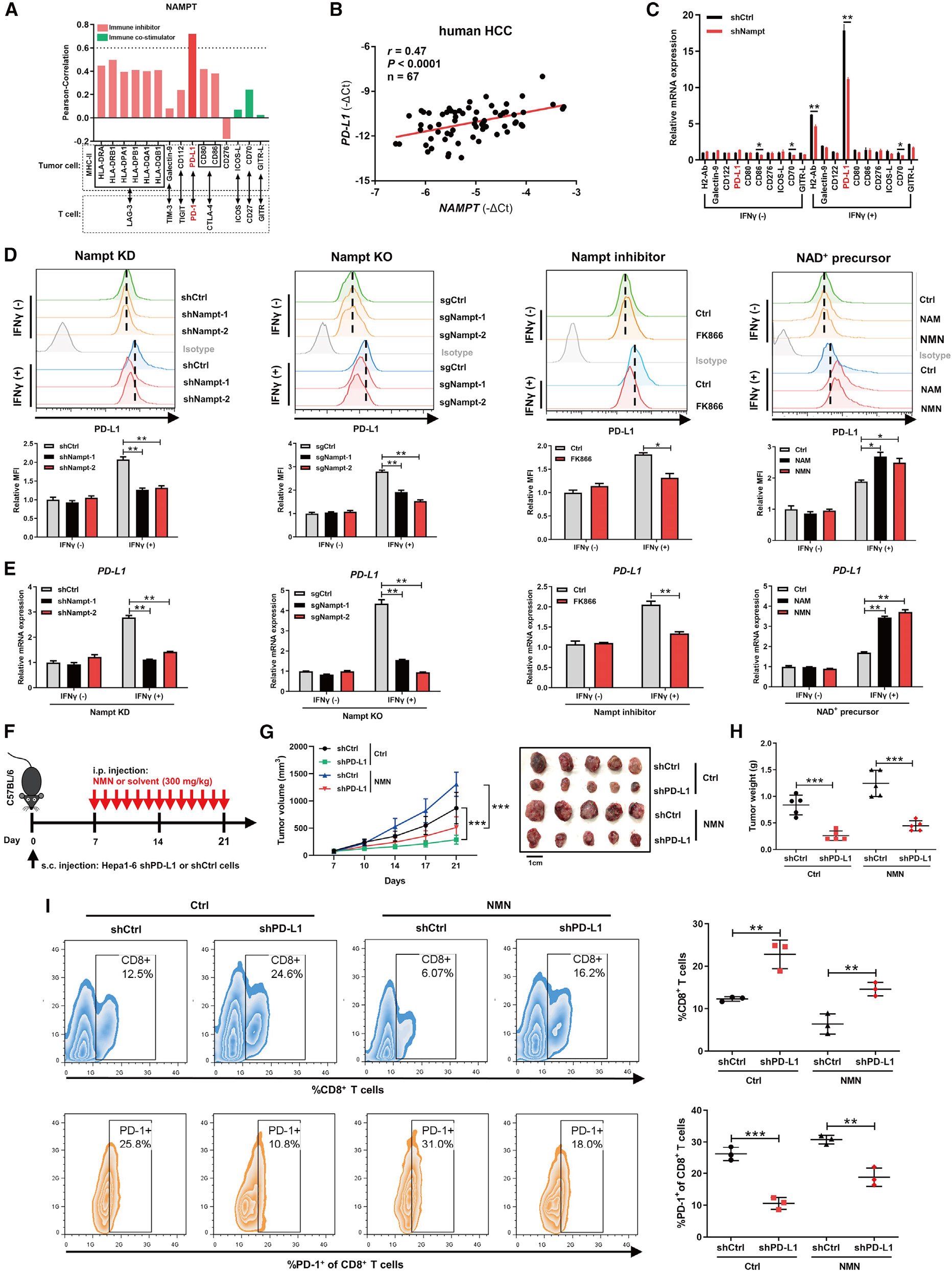
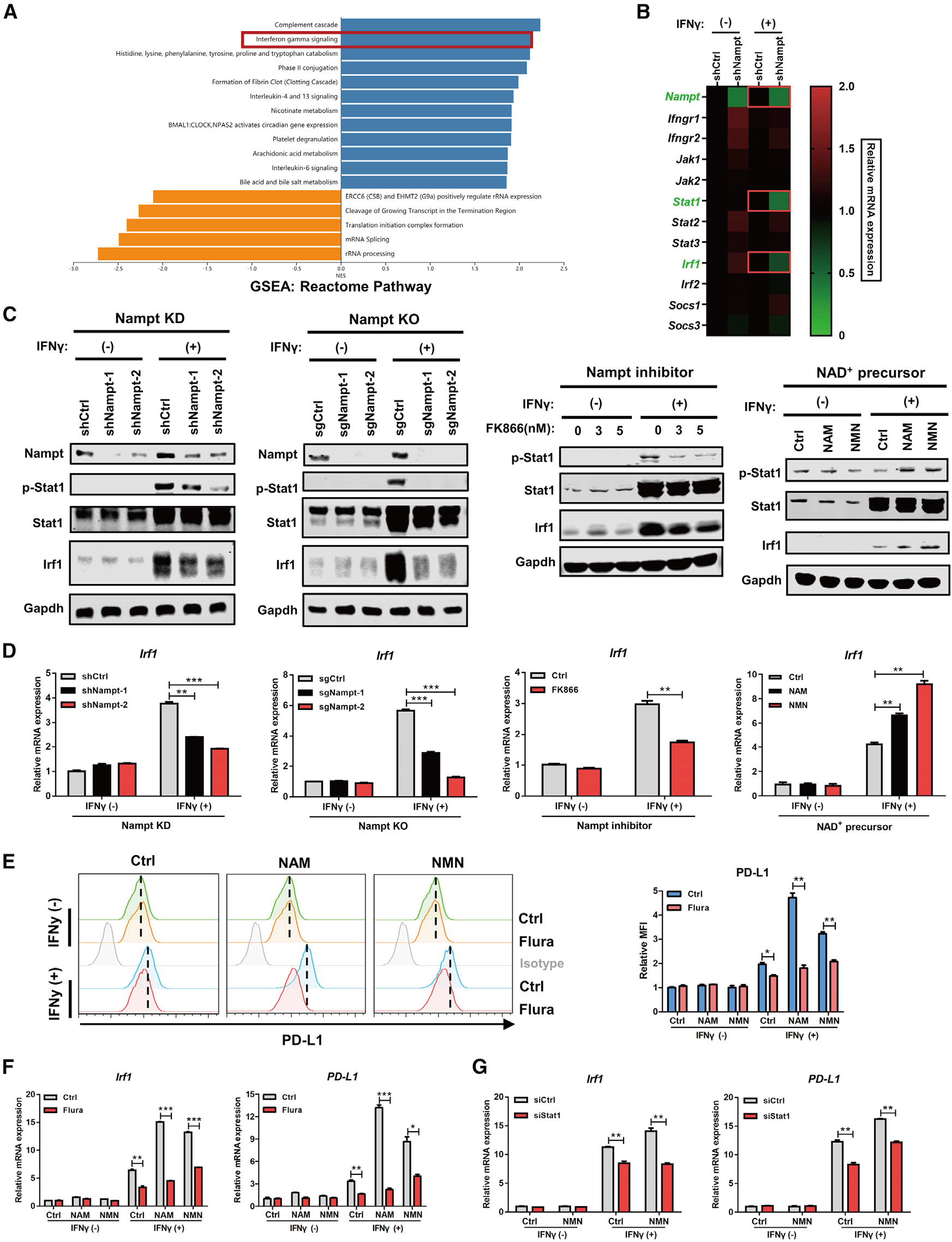
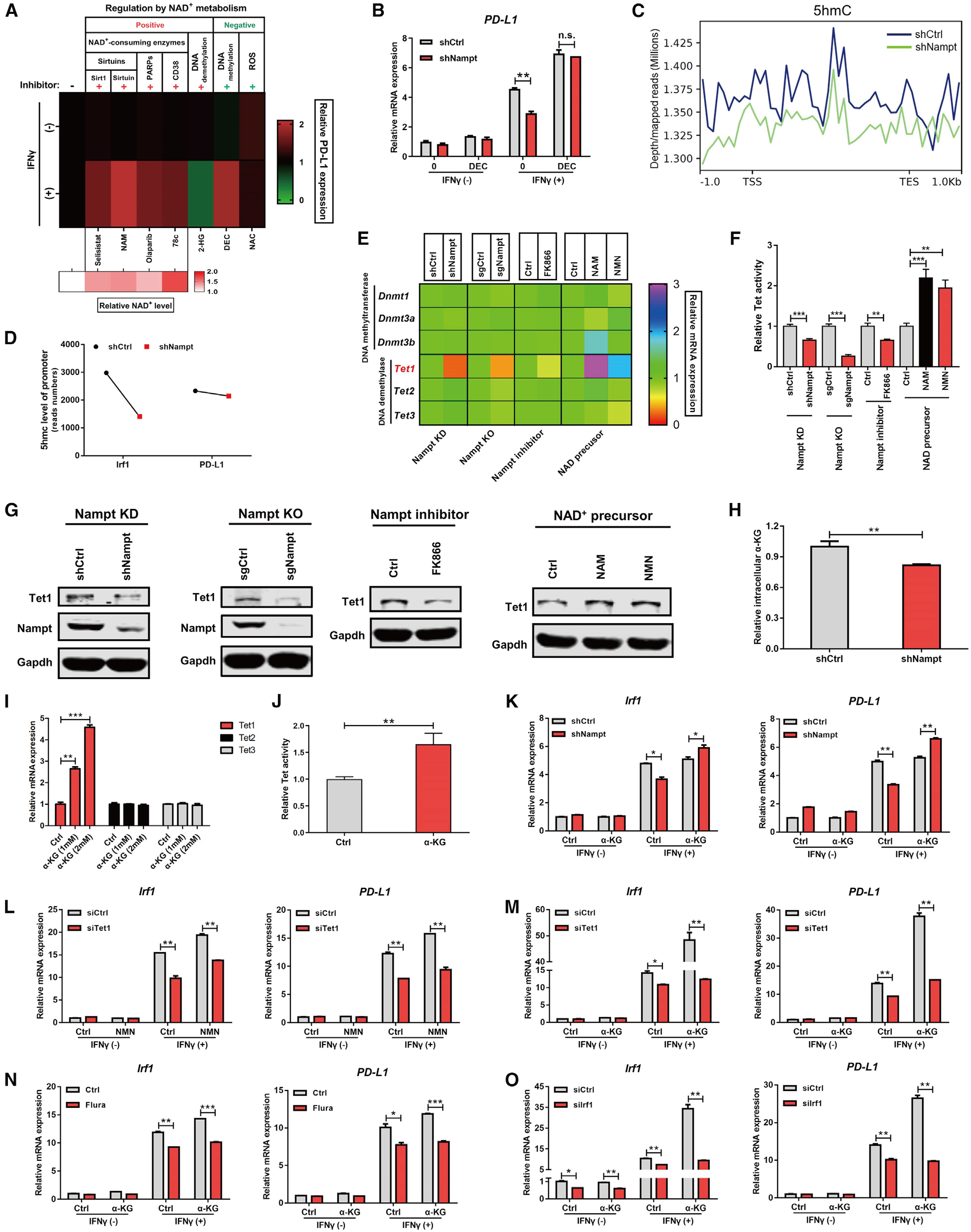
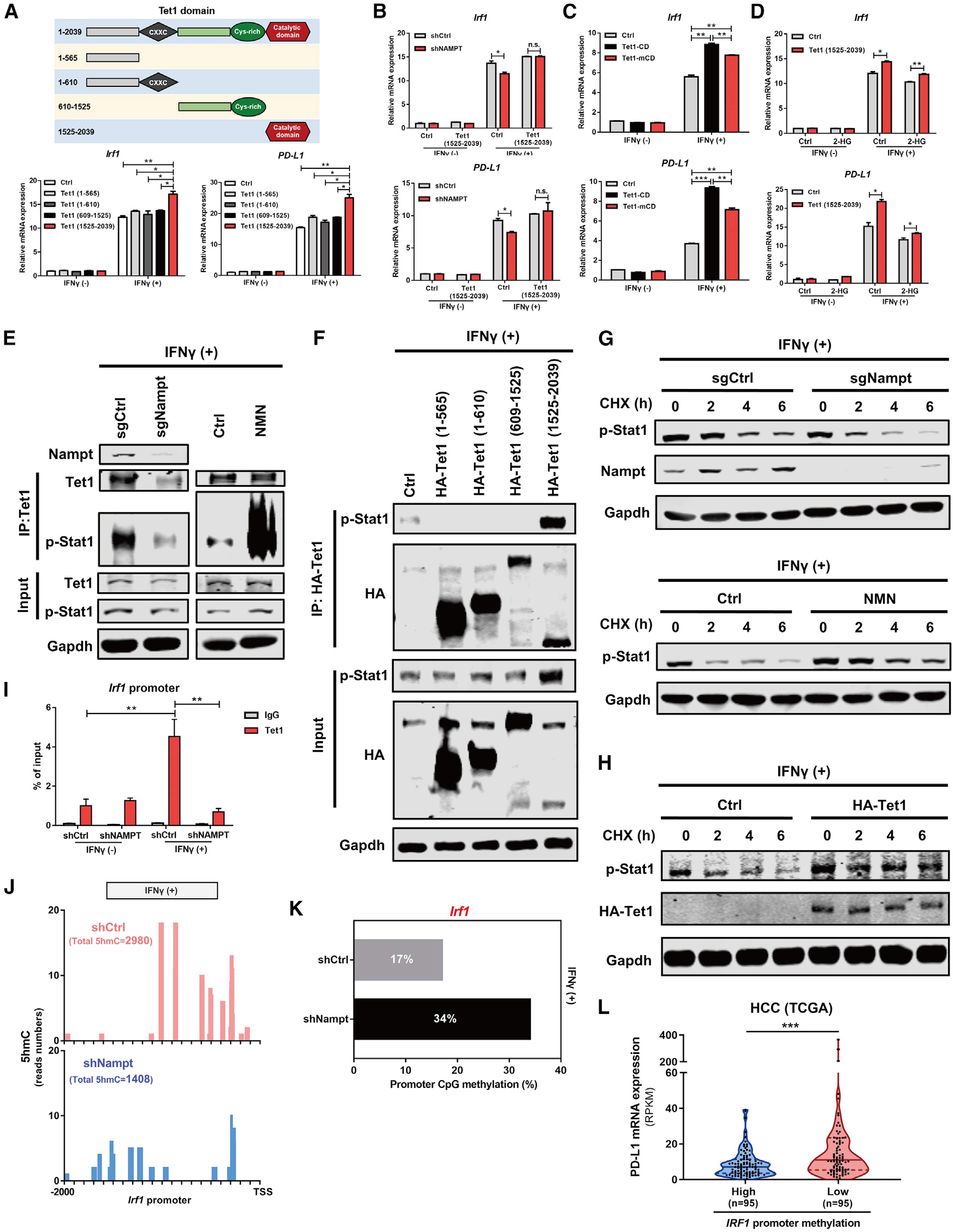

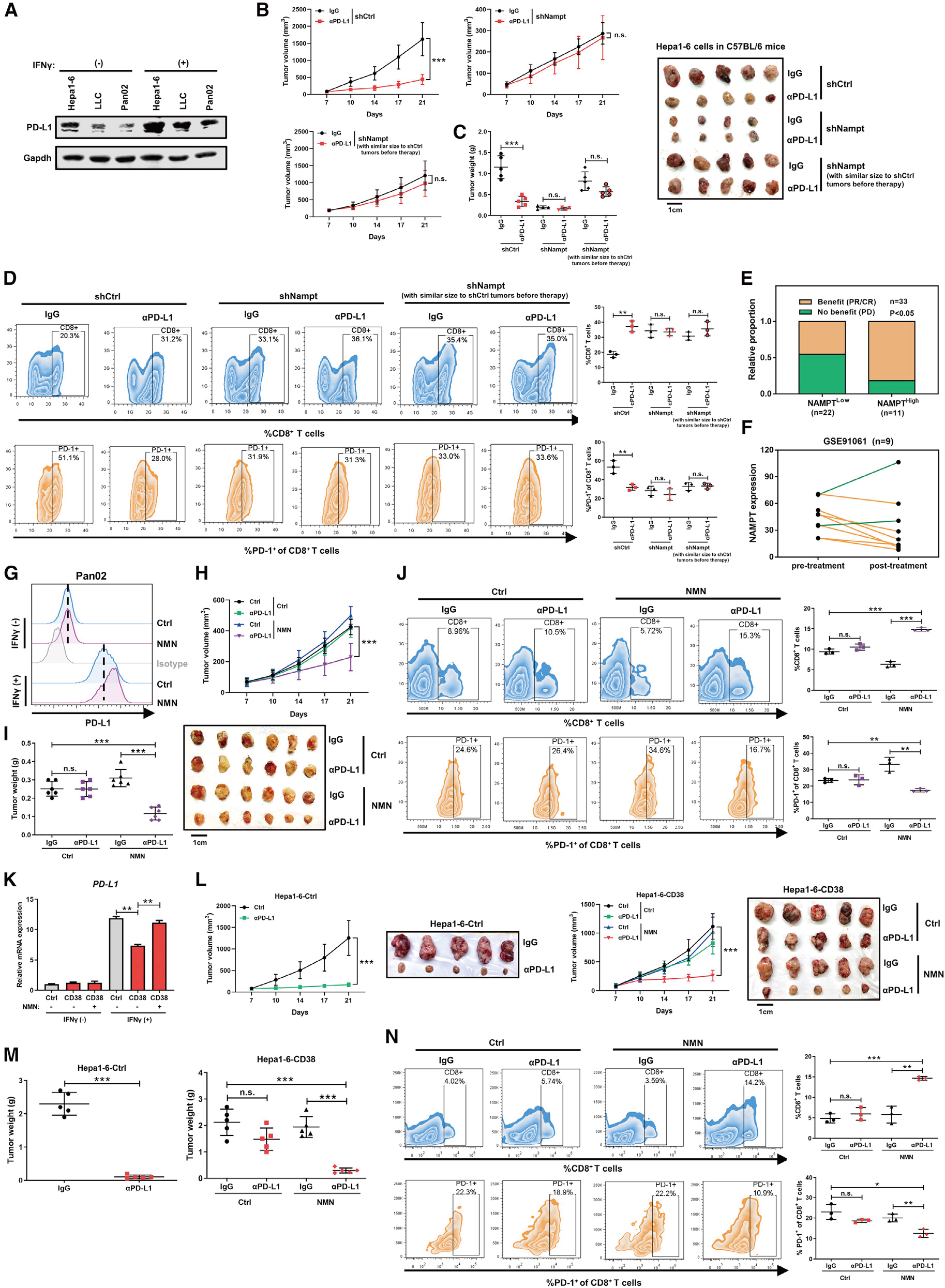
结论:
参考文献:
[1] Cairns, R.A., Harris, I.S., and Mak, T.W. (2011). Regulation of cancer cell metabolism. Nat. Rev. Cancer 11, 85–95.
[2] Verdin, E. (2015). NAD+ in aging, metabolism, and neurodegeneration. Science350,1208–1213.
[3] Nacarelli, T., Lau, L., et al. (2019). NAD+ metabolism governs the proinflammatory senescence-associated secretome. Nat. Cell Biol. 21, 397–407.
[4] Ohaegbulam, K.C., Assal, A., Lazar-Molnar, E., Yao, Y., and Zang, X. (2015).Human cancer immunotherapy with antibodies to the PD-1 and PD-L1 pathway. Trends Mol. Med. 21, 24–33.
[5] Hongwei Lv, Guishuai Lv., et al. (2021). NAD + Metabolism Maintains Inducible PD-L1 Expression to Drive Tumor Immune Evasion. Cell Metab.2021 Jan 5;33(1):110-127.e5.doi: 10.1016/j.cmet.2020.10.021.
更多业务需求可扫描下方二维码,填写表单,我们将尽快安排专人与您联系!


扫一扫,反馈当前页面
和元生物