
Cell | 重磅!磷酸戊糖途径在神经损伤修复中的双重核心作用,脊髓损伤修复迎来全新治疗靶点
神经系统的稳态维持与损伤修复,一直是神经科学领域的核心科学问题与临床难题。成年哺乳动物的周围神经系统(PNS)损伤后,轴突可自发实现再生与功能修复;但中枢神经系统(CNS),尤其是脊髓损伤(SCI)后,轴突再生能力极度受限,会导致患者出现永久性的感觉、运动功能障碍,目前临床上仍无有效的根治手段。尽管学界已对调控轴突再生的转录调控、信号转导通路开展了数十年的深入研究,但决定PNS与CNS再生能力巨大差异的核心代谢机制,长期以来尚未被完全阐明。
·研究结果·
·结论·
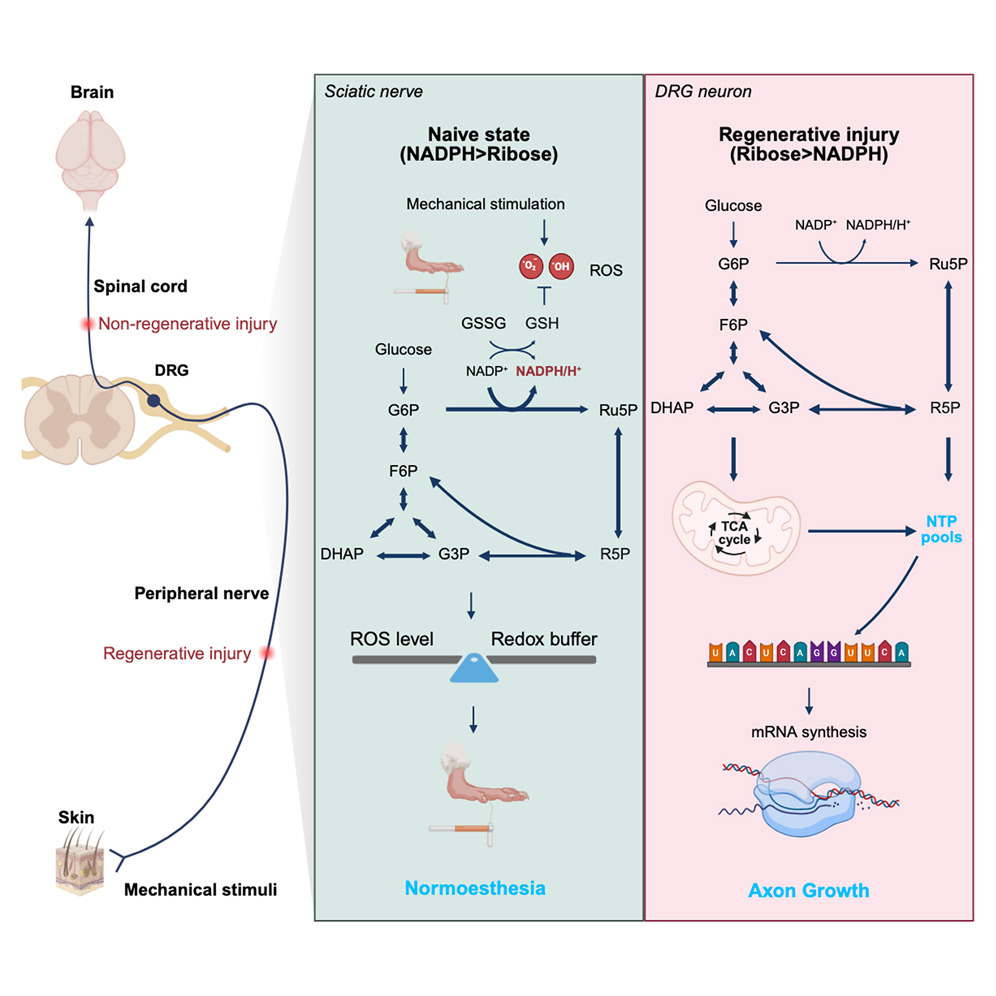
该研究借助多组学分析、基于病毒载体的特异性过表达/敲除、基因编辑和行为学等技术手段首次揭示戊糖磷酸途径作为神经系统感觉稳态和轴突再生的代谢检查点,通过“双重功能”调控生理与修复:生理状态下维持周围轴突氧化还原平衡以支持机械感觉,PNS损伤后激活非氧化分支促进核苷酸合成以驱动再生,而CNS损伤后PPP沉默是再生失败的关键原因。通过TKT过表达或口服D-核糖成功在脊髓损伤模型中重激活PPP通路,实现了感觉与运动轴突的高效再生,以及神经功能的显著恢复。这一发现不仅填补了神经再生领域代谢调控机制的关键空白,更通过两种可临床转化的策略,为脊髓损伤、神经退行性疾病等中枢神经系统疾病的治疗,提供了全新的代谢靶点与干预思路。

扫一扫,反馈当前页面
和元生物