
【Autophagy】科学新发现——吸烟会引起骨质疏松?
镉(Cd)是自然界中普遍存在的一类威胁人类健康的金属元素[1]。中国香烟中的重金属镉含量一直都很高,吸烟人群的血镉浓度高于不吸烟者。近些年的流行病学研究证实,即使低含量的镉暴露会增加骨折和骨质疏松的风险,而超标的镉接触则严重影响人体的健康。
镉增加的骨质疏松和骨折风险是如何发生的呢?大量研究表明自噬在镉诱导的骨毒性中起关键作用[2]。
自噬是一个自身细胞质蛋白或细胞器被包进囊泡,并与溶酶体融合降解其包裹内容物的过程,实现细胞本身的代谢需要和某些细胞器的更新,同时自噬活性过强也会导致细胞的死亡。主要有四个阶段:自噬体产生阶段—形成阶段—成熟阶段—分解阶段。
 自噬发生过程
自噬发生过程
过去的研究对于镉诱导的自噬导致的骨毒性的具体机制尚不清楚,浙江大学的周舟教授和陆军军医大学的余争平教授团队合作的研究成果10月20号在线刊登了在《Autophagy》上。
皮会丰博士等人的研究表明镉诱导TFE3(转录因子E3)介导的骨间充质干细胞(MSCs)发生自噬,发现了PPP3/calcineurin-AKT-TFE3介导的自噬溶酶体作用机制,为今后针对Cd诱导骨毒性的药物治疗开辟了新的前景。
Cd诱导的自噬可以通过吖啶橙染色或者透射电子显微镜检测,同时研究人员检测了自噬接头蛋白SQSTM1/p62 (sequestosome 1)及LC3的水平变化显示Cd可以诱导自噬。该蛋白通过与MAP1LC3/LC3(微管相关蛋白1轻链3)的直接结合,选择性地结合到自噬体中,并通过自噬高效降解。同时干扰自噬相关基因Atg7有效减少Cd诱导的细胞死亡(图1)。
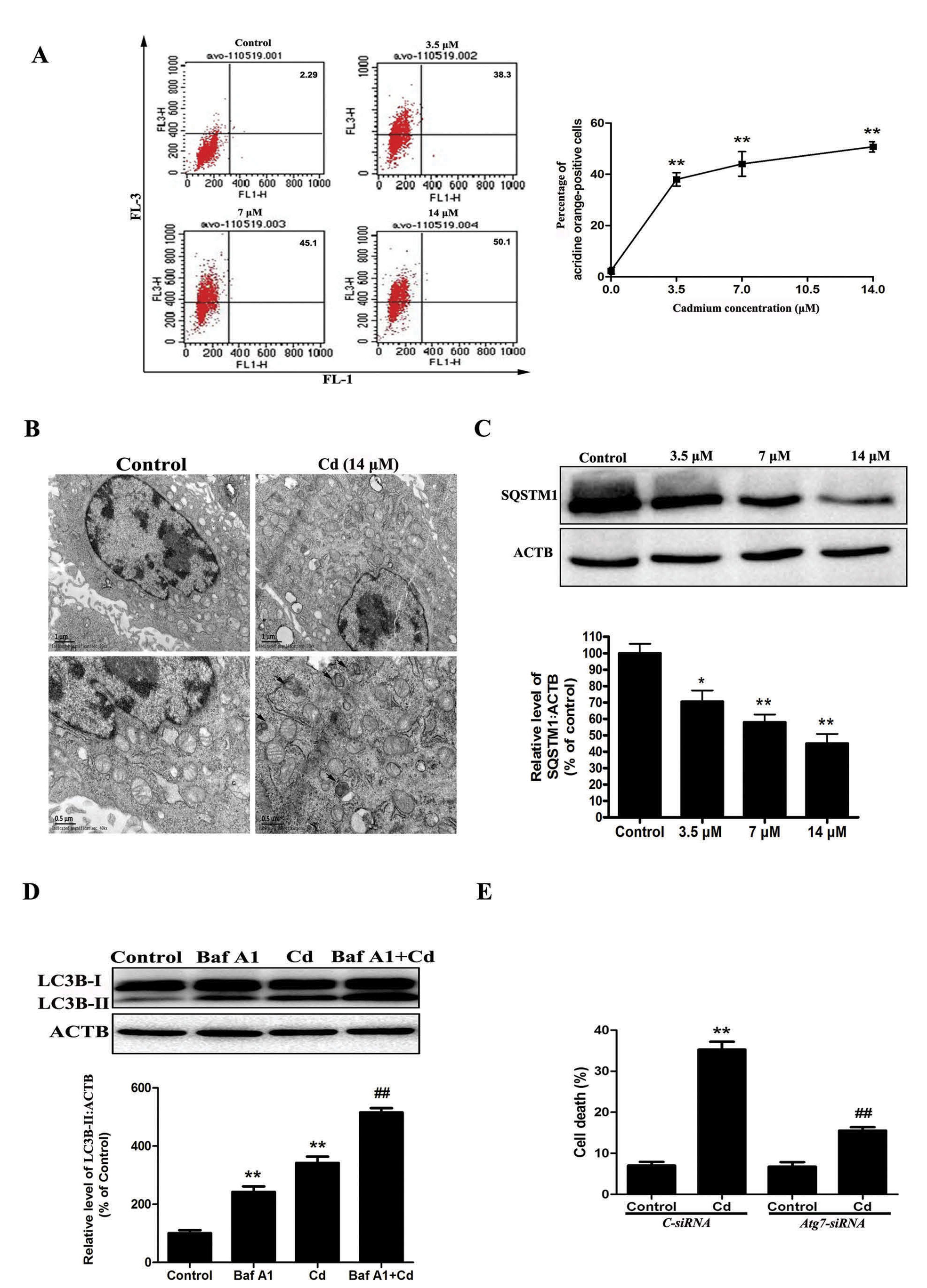 图1 Cd诱导培养的骨间充质干细胞自吞噬死亡
2.Cd诱导培养的MSCs中TFE3的核定位
图1 Cd诱导培养的骨间充质干细胞自吞噬死亡
2.Cd诱导培养的MSCs中TFE3的核定位
TFE3(转录因子E3)是亮氨酸拉链转录因子家族成员,主要调节自噬和溶酶体发生的相关基因的表达[3]。免疫荧光和荧光素酶报告基因检测等实验都证实Cd处理促进TFE3核定位,TFE3激活自噬相关基因的表达(图2)。
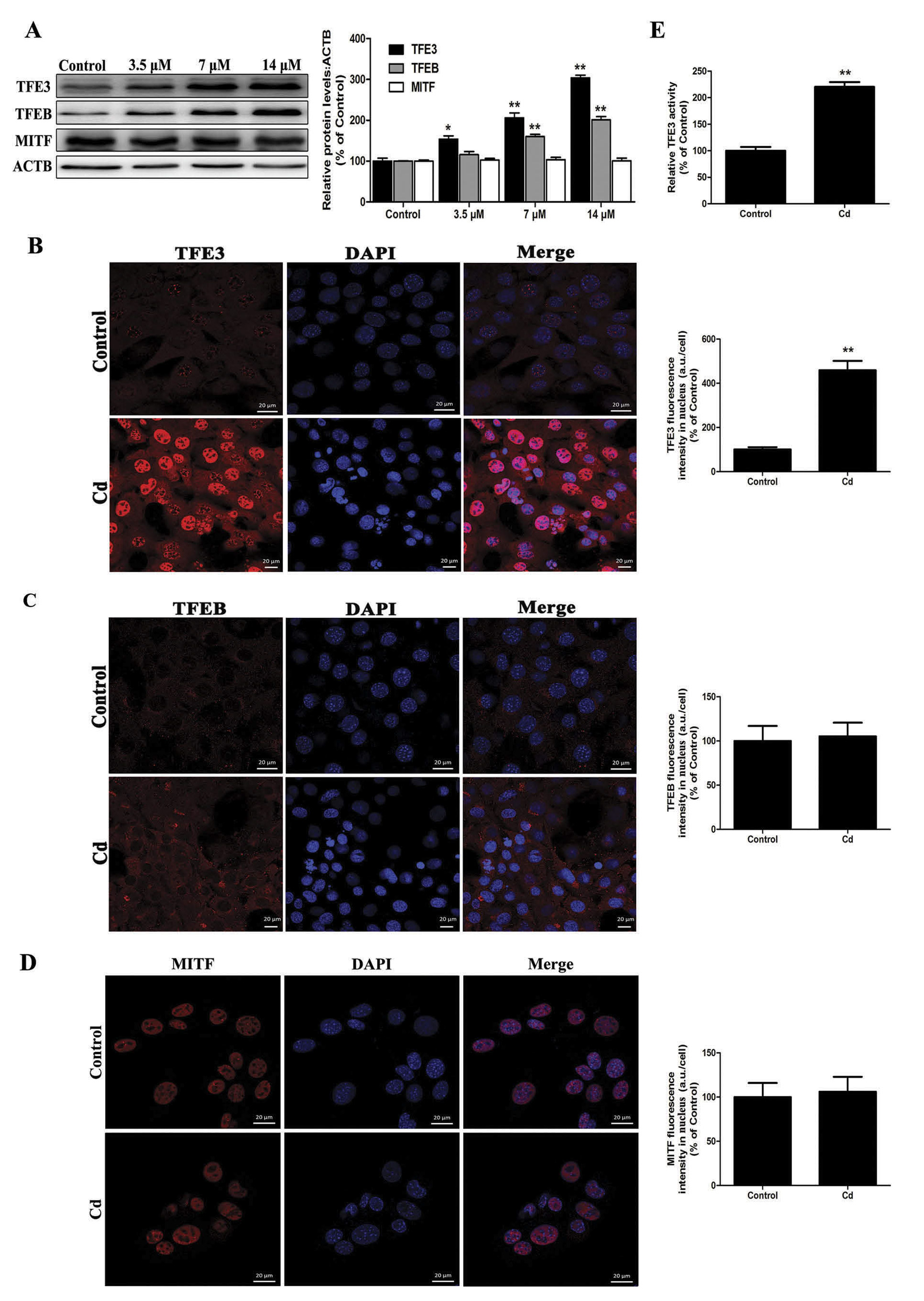 图2 Cd诱导培养的骨间充质干细胞TFE3的核转运 3.Cd激活TFE3诱导MSCs的自噬
图2 Cd诱导培养的骨间充质干细胞TFE3的核转运 3.Cd激活TFE3诱导MSCs的自噬
接下来作者通过特异的siRNA干扰TFE3活性,抑制了Cd诱导MSCs的自噬(图3)。TFE3的转录调控活性依赖于其磷酸化修饰[4],并受对营养和生长因子敏感的信号机制控制,比如mTORC1(雷帕霉素激酶复合体1),通过其磷酸化靶蛋白的检测表明在培养的MSCs中,Cd激活TFE3与MTORC1无关。
 图3 TFE3介导培养的骨髓间充质干细胞中cd诱导的自噬
图3 TFE3介导培养的骨髓间充质干细胞中cd诱导的自噬
研究团队通过AKT(丝氨酸/苏氨酸激酶 )位置权重矩阵 (PWM)扫描TFE3的氨基酸位点,预测出AKT磷酸化TFE3潜在的位点,并进一步验证AKT对TFE3去磷酸化激活的机制,Cd降低了磷酸化AKT(P-AKT)的表达(Ser473)。本底AKT活性的升高增加TFE3在Ser565位点去磷酸化,促进TFE3核定位(图4)。
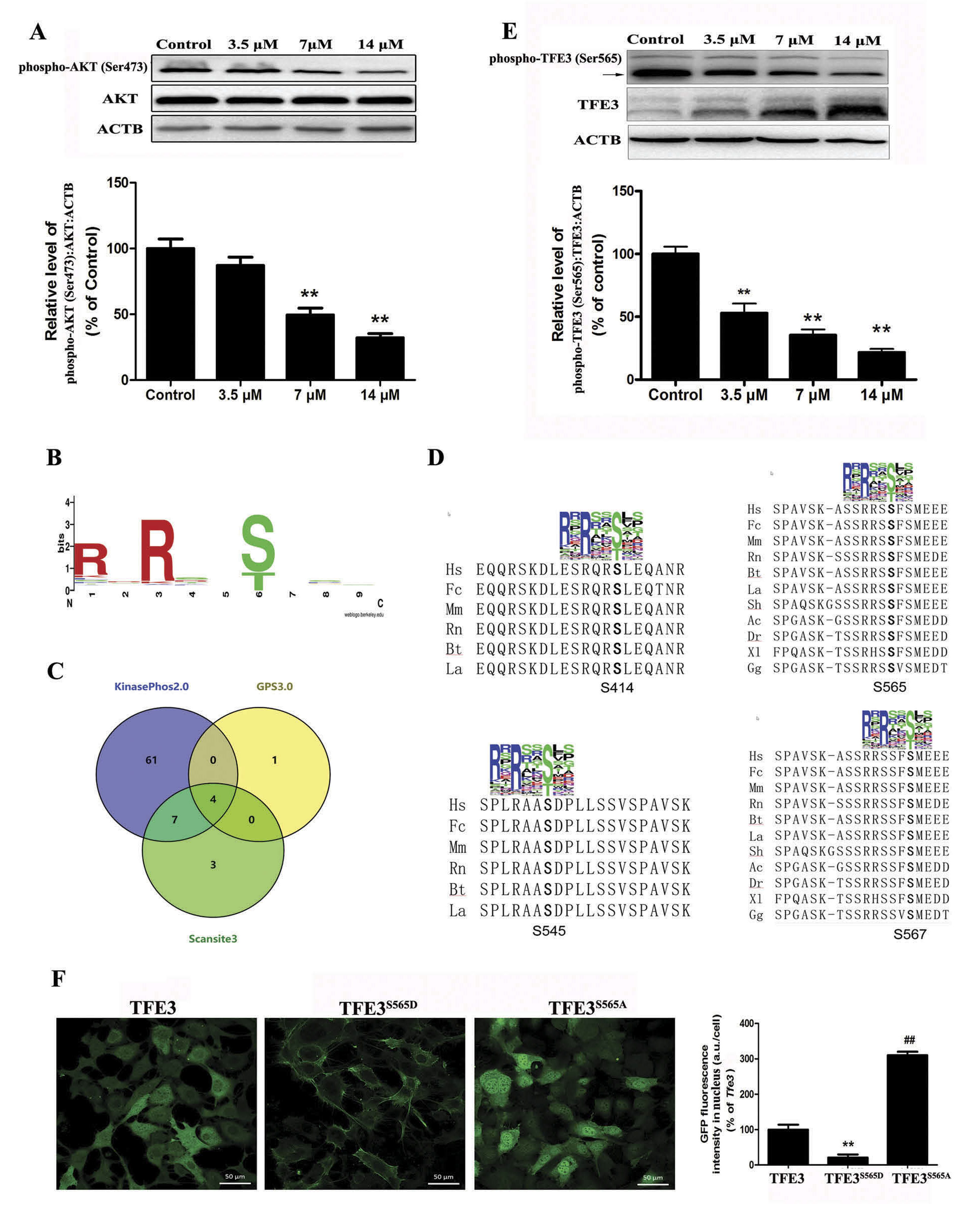 图4 AKT通过磷酸化ser565位点调控TFE3活性
5.AKT-TFE3通路对Cd诱导起重要作用
图4 AKT通过磷酸化ser565位点调控TFE3活性
5.AKT-TFE3通路对Cd诱导起重要作用
蛋白磷酸酶/钙调磷酸酶(PPP3/calcineurin)在调控TFE3中起重要作用,通过负调控AKT的磷酸化作用,而增强AKT对TFE3的去磷酸化激活作用来促进TFE3核转移(图5)。
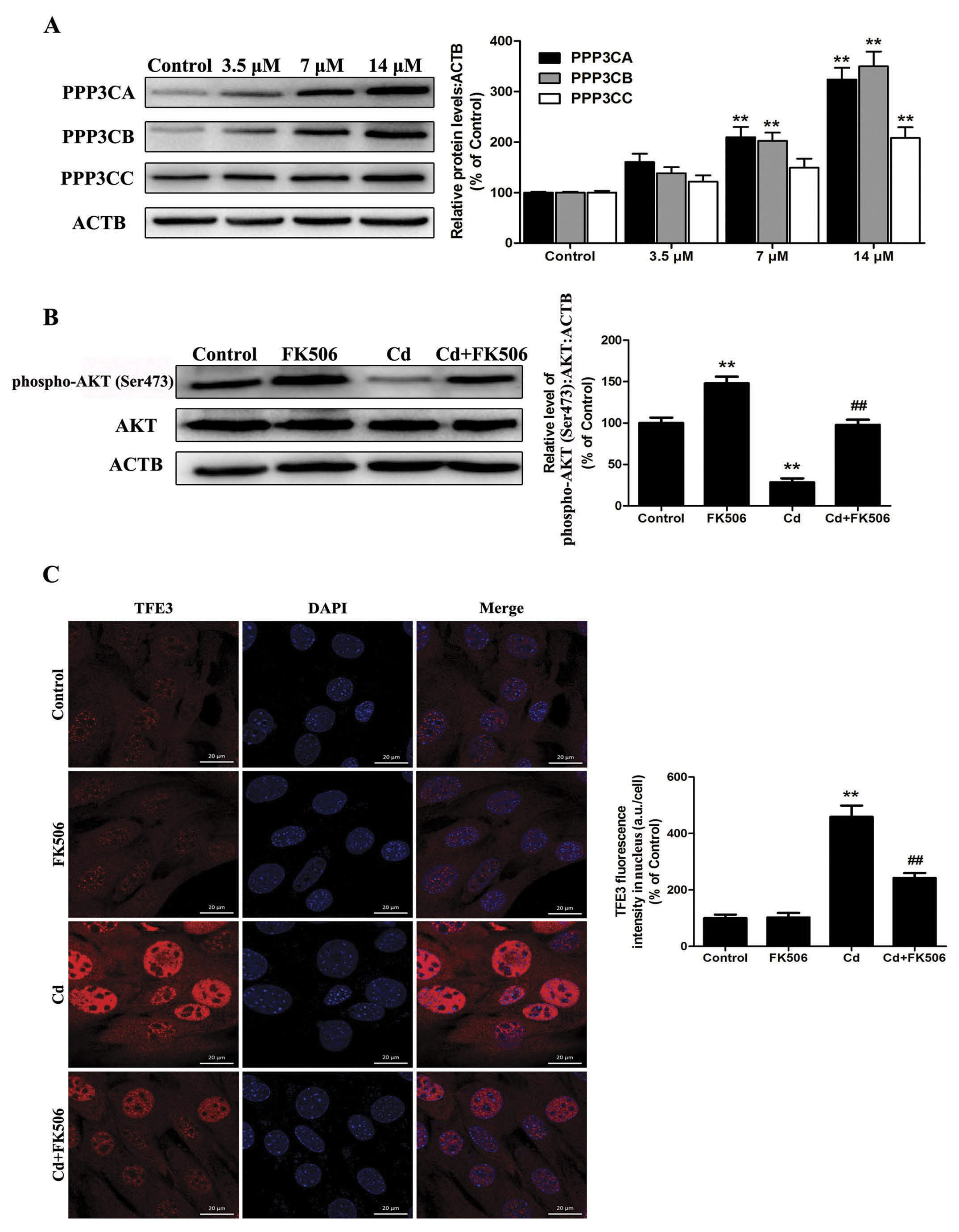 图5 PPP3/calcineurin调控 AKT-TFE3通路对Cd诱导起重要作用
图5 PPP3/calcineurin调控 AKT-TFE3通路对Cd诱导起重要作用
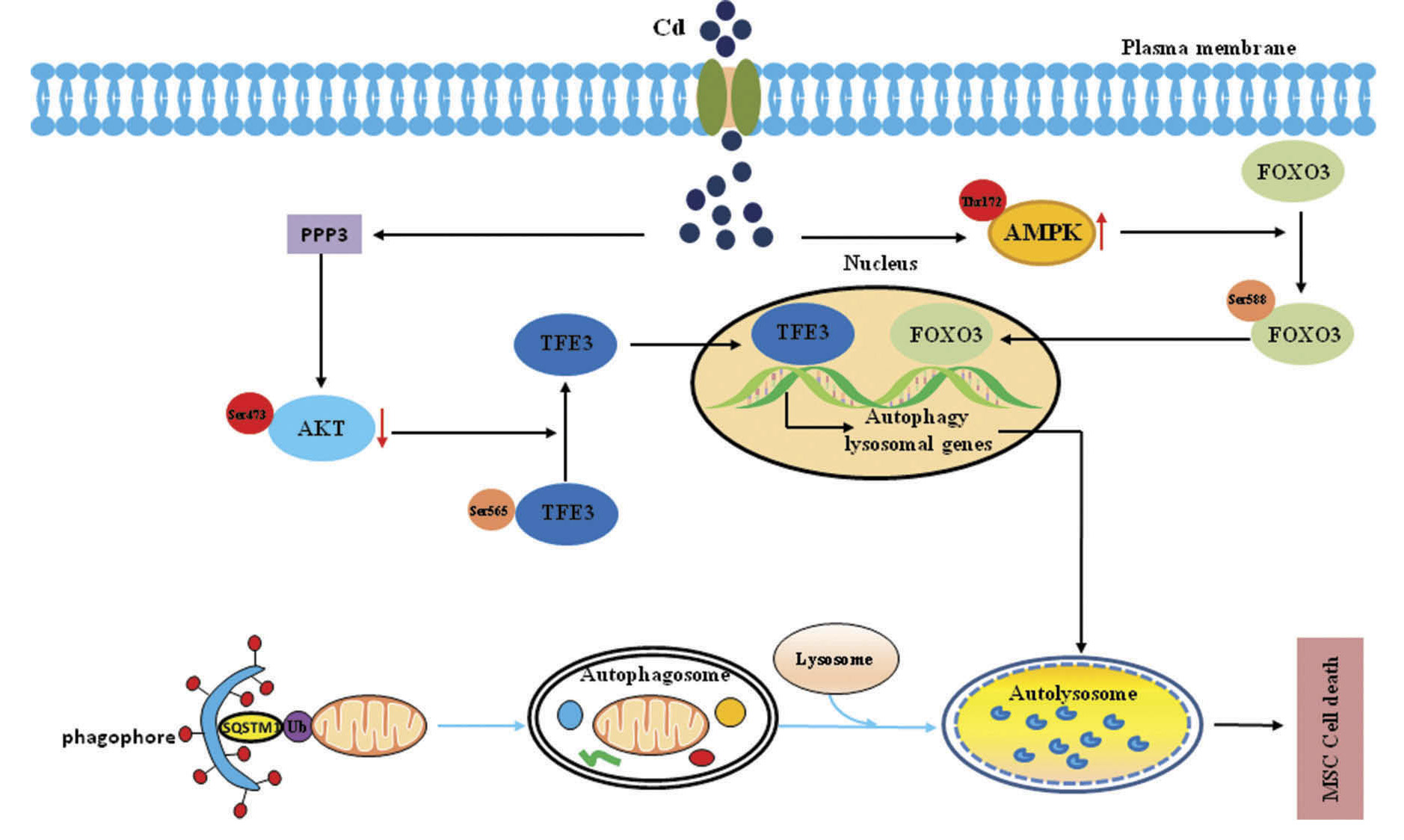 一图读懂在Cd诱导骨间充质干细胞毒性中AKT激活TFE3促进自噬发生机制
一图读懂在Cd诱导骨间充质干细胞毒性中AKT激活TFE3促进自噬发生机制
自噬可通过清除有毒代谢物和细胞内病原体诱导的功能失调或受损的细胞内细胞器来帮助细胞存活,而过度的自噬激活会引发自噬程序性细胞死亡,通过过表达、干扰或基于病毒载体进行相关信号通路基因一系列操作,证实自噬主要参与了Cd介导的骨毒性。PPP3/calcineurin-AKT-TFE3通路调控自噬溶酶体机制为Cd诱导骨损伤的治疗提供新的治疗方法。
参考文献:
[1]Chen X, Ren S, Zhu G, et al. Emodin suppresses cadmiuminduced osteoporosis by inhibiting osteoclast formation. Environ Toxicol Pharmacol. 2017;54:162–168.
[2]Chen X, Wang K, Wang Z, et al. Effects of lead and cadmium coexposure on bone mineral density in a Chinese population. Bone.2014;63:76–80.
[3]Perera RM, Stoykova S, Nicolay BN, et al. Transcriptional control of autophagy-lysosome function drives pancreatic cancer metabolism.Nature. 2015 Aug 20;524(7565):361–365.
[4]Palmieri M, Pal R, Nelvagal HR, et al. mTORC1-independent TFEB activation via Akt inhibition promotes cellular clearance in neurodegenerative storage diseases. Nat Commun. 2017 Feb06;8:14338。

扫一扫,反馈当前页面
和元生物