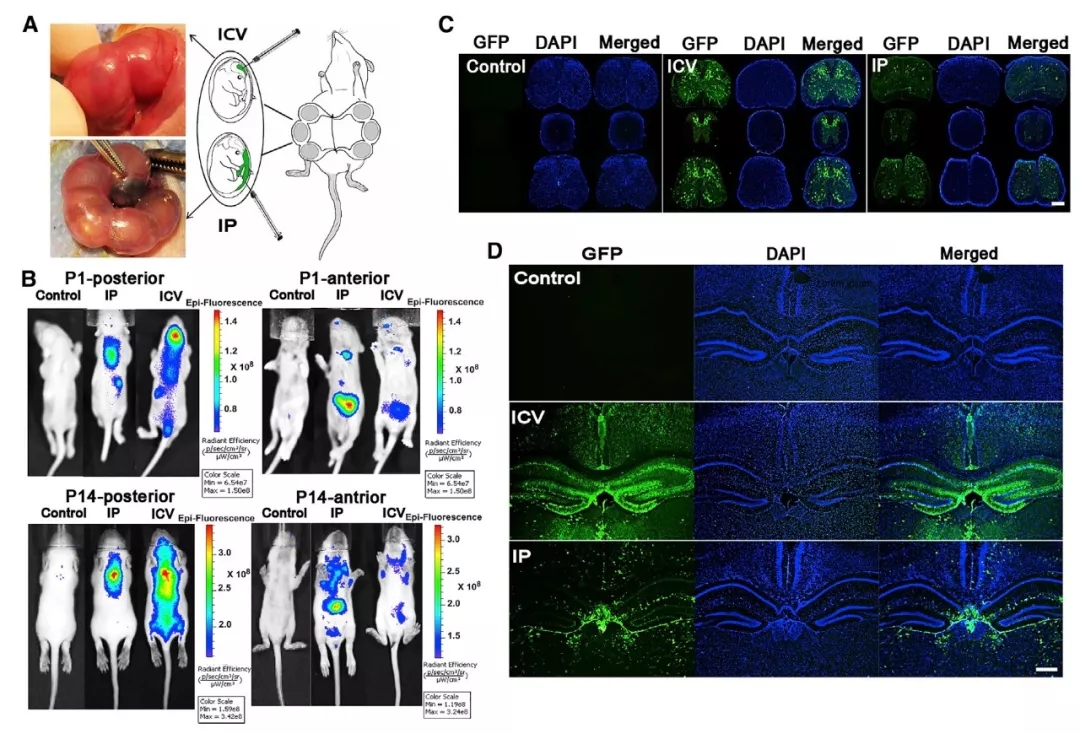
进一步的研究发现,相较于胎盘注射,将AAV9-EGFP通过侧脑室注射,使荧光蛋白在小鼠皮层神经元和脊髓运动神经元上的表达较高,提示了通过侧脑室注射,AAV9-EGFP更倾向于感染神经元(图2)。
随后,研究人员借助Western blot分析发现,通过侧脑室注射使EGFP蛋白在脊髓、皮层、海马等脑区的表达量明显高于胎盘注射的,然而,在丘脑的表达量明显低于胎盘注射的,提示了将病毒载体介导的EGFP蛋白通过侧脑室注射到胎儿的大脑中,该病毒进入脑脊液(CSF),并以很高的效率转导大脑及脊髓中的神经元(图3A,C)。在其他脏器中,侧脑室注射介导EGFP蛋白在肝脏和棕色脂肪组织(BAT)等脏器组织的表达量明显低于胎盘注射的。
为了研究SMA疾病的胎儿基因治疗,研究人员在小鼠胚胎时期(E14.5-E15)侧脑室注射两种rAAV基因治疗载体:单链rAAV(ssAAV)和双链rAAV(scAAV)载体携带的SMN基因(rAAV9-SMN),并监测了接受侧脑室注射治疗后小鼠的存活率及足月出生小鼠的体重和寿命(图4A,B)。结果发现,未接受治疗的SMA小鼠存活率最低(存活寿命不超过14天),rAAV载体携带SMN基因的治疗组小鼠存活寿命显著延长,但仍短于野生型健康小鼠(图4B)。此外,接受基因治疗的小鼠比SMA小鼠体重更重,且略低于健康小鼠的体重(图4C)。
scAAV,是一个互补的(self-complementary)双链分子,不必像传统的ssAAV经过基因组的第二链合成才能启动基因的转录,跳过合成双链这一限速步骤,直接编码SMN蛋白,快速高效起效。
结论
随着胎儿基因组分析的最新进展,医生可以在出生前检测出基因异常,早期发现可使治疗计划在产前或出生后不久实施。此外,基于胎儿的特殊生理特征,比如体内的干细胞有多项分化潜能、胎儿体积小及其免疫系统尚不健全等为基因治疗提供了独特的条件,利用产前基因治疗可以将治疗基因转染到胎儿,可使许多疾病在发病前得以治愈,这对于一些早发性遗传性疾病可能是最佳的治疗手段。目前,产前筛查技术的进步和基因传递技术的突破为胎儿基因治疗研究铺平了道路。
在本项研究中,研究人员将目光聚焦产前基因治疗,他们借助病毒载体递送技术、分子生物学技术等手段发现,将rAAV9-SMN通过侧脑室方式注射到胚胎期小鼠体内,借助rAAV9病毒载体可高效地将SMN基因递送到小鼠大脑、脊髓等部位,实现有效延长出生后小鼠的寿命,增加运动神经元数量,改善肌肉萎缩现象。这一研究成果为胎儿基因治疗SMA提供了有效的基础研究支持,是胎儿基因治疗取得的一个重要进展。
和元生物 是一家集基础研究服务、基因治疗药物载体开发和临床级重组病毒产业化制备三大发展方向于一体的高新技术企业。以“打造一个平台,推动一个行业”为战略目标,和元生物 长期致力于病毒载体的创新和产业化推进,已拥有基因治疗载体研发中心、SPF级动物实验室、中试工艺开发与生产实验室以及基于一次性技术的GMP级重组病毒车间。和元生物 始终坚持以基因治疗重组病毒载体研发及生产为核心,发展成为辐射全球的重组病毒药物生产CRO服务中心和基因药物生产CDMO/CMO基地。