
【血友病连载】A型血友病的基因治疗疗法盘点
昨天是世界献血者日,每年的6.14日,世界各国庆祝世界献血者日,希望通过这个活动来感谢自愿无偿献血者献出可挽救生命的礼物——血液,同时提高人们对定期献血必要性的认识,以确保个人和社区都可及时获得负担得起的安全和有质量保证的血液和血液制品。
在鲜血的类型中,成分输血是现代输血的新理念。成分献血是治疗血友病的重要手段之一,当病人由各种原因造成血小板减少或血小板功能异常而引起严重出血时,必须输注血小板来维持凝血功能。近期,OBiO GeneTherapy小编为大家详细介绍了血友病的概况和分类。本期开始,小编将逐一梳理不同血友病的基因治疗疗法,帮助社会各界了解基因治疗治愈血友病的机会,本期首先介绍A型血友病及其基因治疗。
A型血友病是一种由凝血因子VIII缺乏导致的血友病类型,是临床上最常见的血友病,约占血友病人数的80%-85%,而大约三分之一的A型血友病病例是自发基因突变导致的。凝血因子VIII也称为anti-hemoplytic factor/antihemophilic factor (AHF)或globulin (AHG)/antihemophilic factor A,产生于血管内皮细胞。
A型血友病是一种遗传性疾病,但已知病例中约有三分之一是由自发的基因突变引起的,超过一半的A型血友病患者病情严重。A型血友病的遗传信息由X染色体携带,以X连锁的隐性方式遗传疾病。因此,女性必须遗传两条携带血友病突变基因的X染色体才会患病,而男性只要携带一条有问题的X染色体即患病。
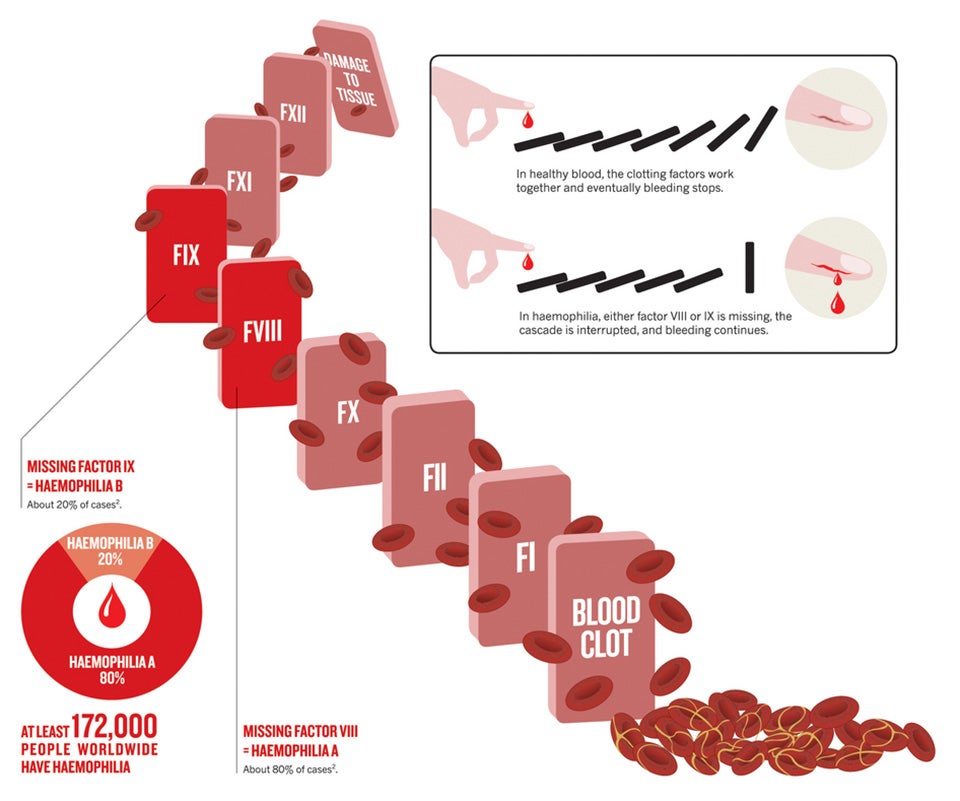
根据血液中凝血因子VIII的比例,A型血友病有三个阶段:轻度、中度和重度。轻度A型血友病患者一般只在严重受伤、创伤或手术后出血,且该疾病是在上述情况之一后、由于长期出血而被诊断出来的,凝血因子VIII的含量是正常水平的6%-49%;中度血友病患者在不太严重的损伤后更容易出血,甚至是自发出血,在严重的情况下,关节和肌肉可能会自发出血,凝血因子VIII的含量是正常水平的1%-5%;重度A型血友病患者凝血因子VIII的含量小于正常水平的1%,该疾病非常凶险。
A型血友病是一种可治疗的疾病,有不同的治疗方法。替代疗法(替换缺失的凝血因子VIII以防止并发症)是目前应用最为广泛的疗法,通常效果良好。一些病情较轻的患者也可以用去氨加压素(desmopressin)治疗,它会提高血液中所有凝血因子的水平。此外,抗纤溶药(Antifibrinolytics)可以减缓血液中凝血因子的分解,用于治疗较温和的A型血友病。
对于严重的A型血友病患者,他们可能需要定期注射凝血因子VIII以防止出血,这种方法称为预防性治疗,此种疗法通常在出血发作后的一个小时内效果最好,因而患者常被训练完成居家治疗。
随着基因治疗概念的发展和疗法开发,基因治疗作为一次治疗、长期甚至终身治愈的潜在疗法被广泛关注。
根据和元生物 市场部不完全统计,目前全球进展到临床阶段的、针对A型血友病的基因治疗疗法至少7种以上:
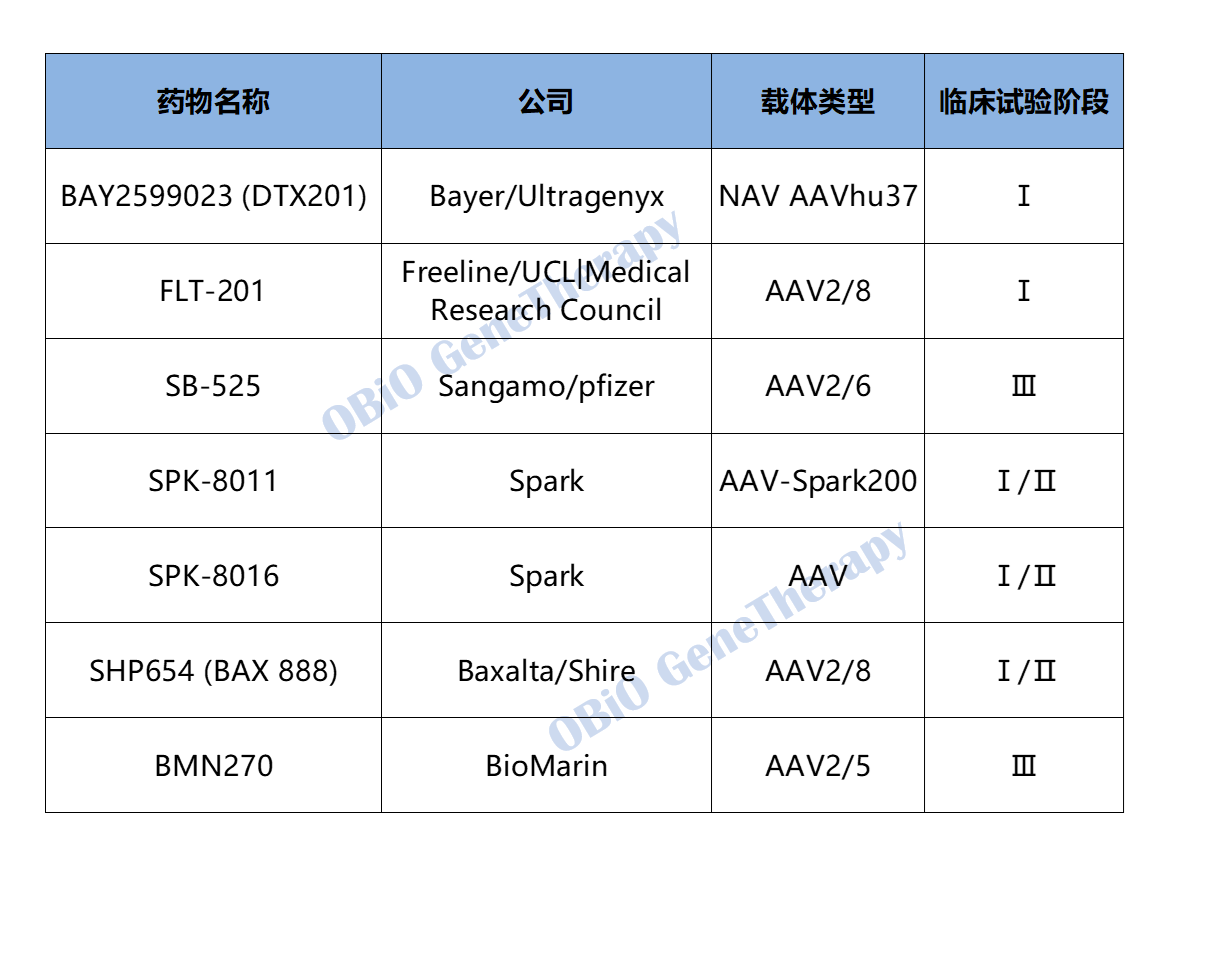
所有疗法均借助腺相关病毒载体完成,数款产品也已进入临床III期,我们有望快速看到A型血友病治疗方案上市应用,现就这些疗法中的代表案例进行简单介绍。

SHP654是由Shire公司/Baxalta公司共同开发的基因疗法,她利用腺相关病毒血清型8(AAV2/8)载体,将一种经过密码子优化的、B结构域删除的凝血因子VIII(BDD-FVIII)专门递送至患者肝脏,之后在肝脏细胞中表达出凝血因子VIII并用于控制出血。该公司在2017年底启动一项I/II期临床研究,评估SHP654的安全性以及用于提高凝血因子VIII活性水平并影响血友病出血的最佳给药剂量。
美国食品和药物管理局(FDA)已授予实验性凝血因子VIII(FVIII)基因疗法SHP654治疗A型血友病的孤儿药地位

FLT210是Freeline公司开发的、用于治疗A型血友病患者的新一代AAV基因疗法。
过去,AAV载体用于A型血友病基因治疗的用途受限于凝血因子VIII的低效表达和大尺寸的凝血因子VIII基因容量过大问题。为了解决这个问题,Freeline开发了两个AAV-凝血因子VIII表达盒,其中含有一个小的合成肝特异性启动子以驱动密码子优化的凝血因子VIII变体的表达。目前该疗法处于临床前试验阶段,拟进行IND申报。
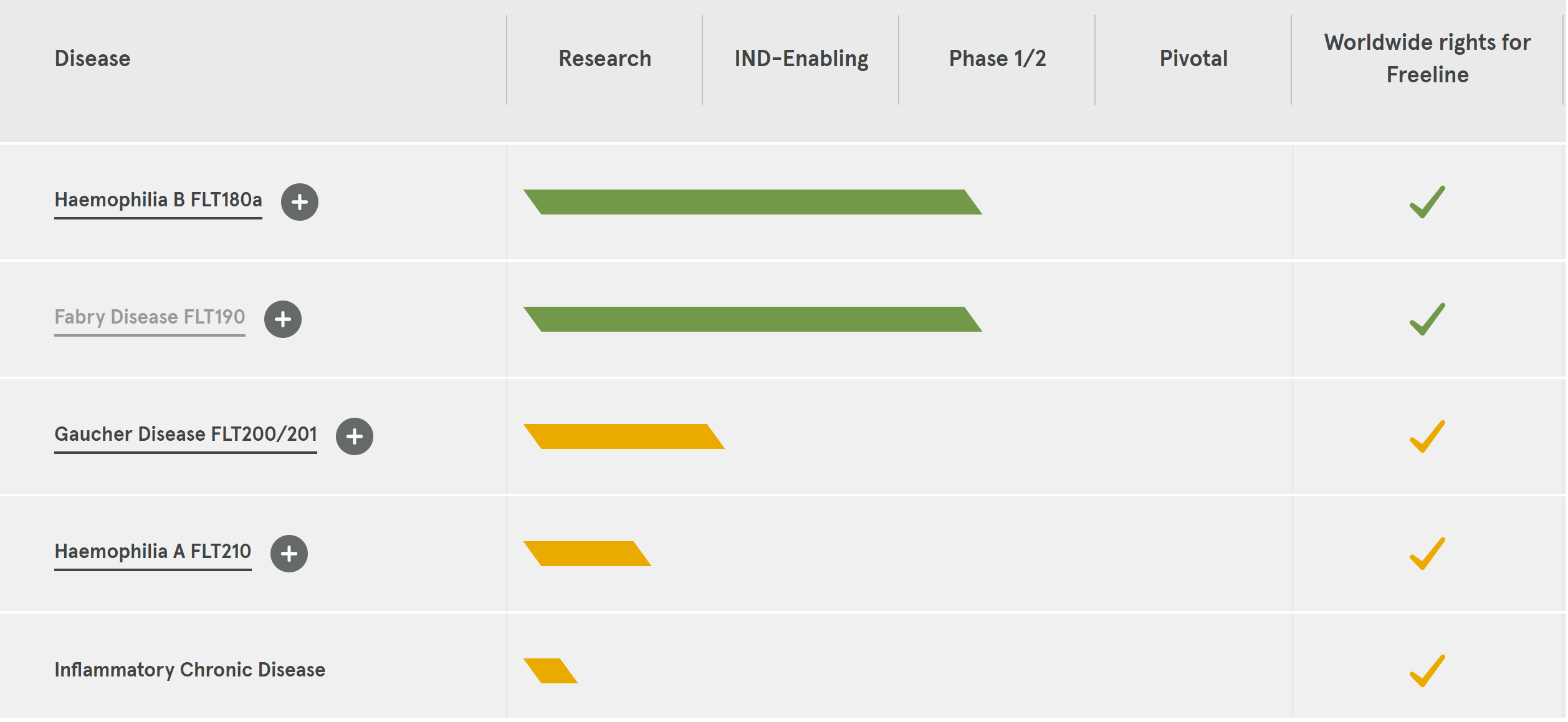
Freeline Therapeutics是一家生物制药公司,成立于2015年,开发用于治疗出血性疾病和其他疾病的基因治疗,其疗法基于下一代专有AAV载体平台,其领先计划是治疗血友病B的基因疗法。 2018年,Freeline完成B轮8800万英镑的融资,由Syncona Ltd牵头(承诺投资8500万英镑),UCL技术基金承诺投资340万英镑。

2018年8月,Ultragenyx宣布与拜耳合作开发用于治疗A型血友病的基因疗法BAY2599023 (DTX201)。DTX201使用REGENXBIO专有的NAV AAVhu37载体,向肝细胞传递凝血因子VIII基因,促进其持续表达,以潜在地克服A型血友病患者的缺陷。该基因疗法来自最初由Dimension Therapeutics研发,并且通过与于2014年拜耳推出最高达2.52亿美元的合作进行开发和商业化。2017年10月,Ultragenyx宣布以1.51亿美元收购Dimension。

SPK-8011是Spark Therapeutics公司开发的一种治疗A型血友病的试验性基因疗法。SPK-8011疗法借助AAV-Spark200病毒载体,携带人凝血因子VIII基因,通过静脉注射,在患者肝脏产生凝血因子VIII。
在I/II期开放标签非随机临床试验(NCT03003533)中,12名凝血因子VIII活性水平低于正常水平的2%的A型血友病患者单次输注三剂SPK-8011(2名患者接受了低剂量的SPK-8011, 3名患者接受了中剂量,7名接受了高剂量),随访52周,以研究凝血因子VIII活性水平变化,并记录任何不良事件。
46周时,所有三种剂量的治疗均减少了94%的出血和95%的凝血因子VIII输注。5名接受高剂量SPK-8011治疗的患者显示出显著的凝血因子VIII活性,出血减少100%,所需凝血因子VIII注射减少99%。高剂量组的两位患者凝血因子VIII水平降到5%以下,可能是因为他们体内对病毒的免疫反应导致。其中一名患者由于凝血因子VIII活性降低而需要住院,这被列为严重不良事件。
Spark Therapeutics正在邀请A型血友病患者参加一项多中心观察性临床研究(NCT03432520),其中约100名患者接受了单剂量SPK-8011,将接受长达5年的随访。这项旨在评估SPK-8011对A型血友病患者的长期安全性和有效性的研究始于2018年8月,计划于2022年12月完成。

SPK-8016是由Spark Therapeutics公司开发的用于治疗产生凝血因子VIII抗体的A型血友病患者的试验性基因疗法。近30%的A型血友病患者在接受血浆来源的或重组的凝血因子VIII注射后会产生抑制性抗体,从而导致治疗无效。
SPK-8016同样借助人工构建的AAV载体,在体内表达可抑制凝血因子VIII抑制性抗体的蛋白,从而有望中和抑制性抗体、提高患者体内的凝血因子VIII水平或活性,恢复正常的凝血途径。
目前,Spark Therapeutics正在招募30名重度A型血友病患者(血液中含有或不含有VIII因子抑制剂的患者)进行I/II期、多中心、开放标签和非随机两部分临床试验(NCT03734588)。
第一部分将评估SPK-8016治疗方案在血液中无可测量凝血因子VIII抑制性抗体的患者中的安全性、有效性和耐受性。第一部分的数据将有助于确定第二部分试验的最佳剂量和研究设计。第二部分中,SPK-8016将在血液中含有凝血因子VIII抑制性抗体的患者中进行测试。
治疗后,患者将被随访52周,评估治疗相关副作用、肝功能、自发和创伤性出血事件的数目、需要注射凝血因子VIII的数量、峰值和稳态凝血因子VIII的活性水平等。这项研究正在美国的密西西比高等医学中心、费城儿童医院和弗吉尼亚联邦大学医学院进行。

SB-525(PF 07055480)是一款基于重组AAV2/6载体的基因疗法,由Sangamo与Pfizer共同开发。它的设计对肝脏特异性启动子、编码因子VIII的转基因,以及polyA和病毒载体序列都作出了改进,不但能够优化载体生产的效率,而且提高肝脏特异性因子VIII蛋白的表达。
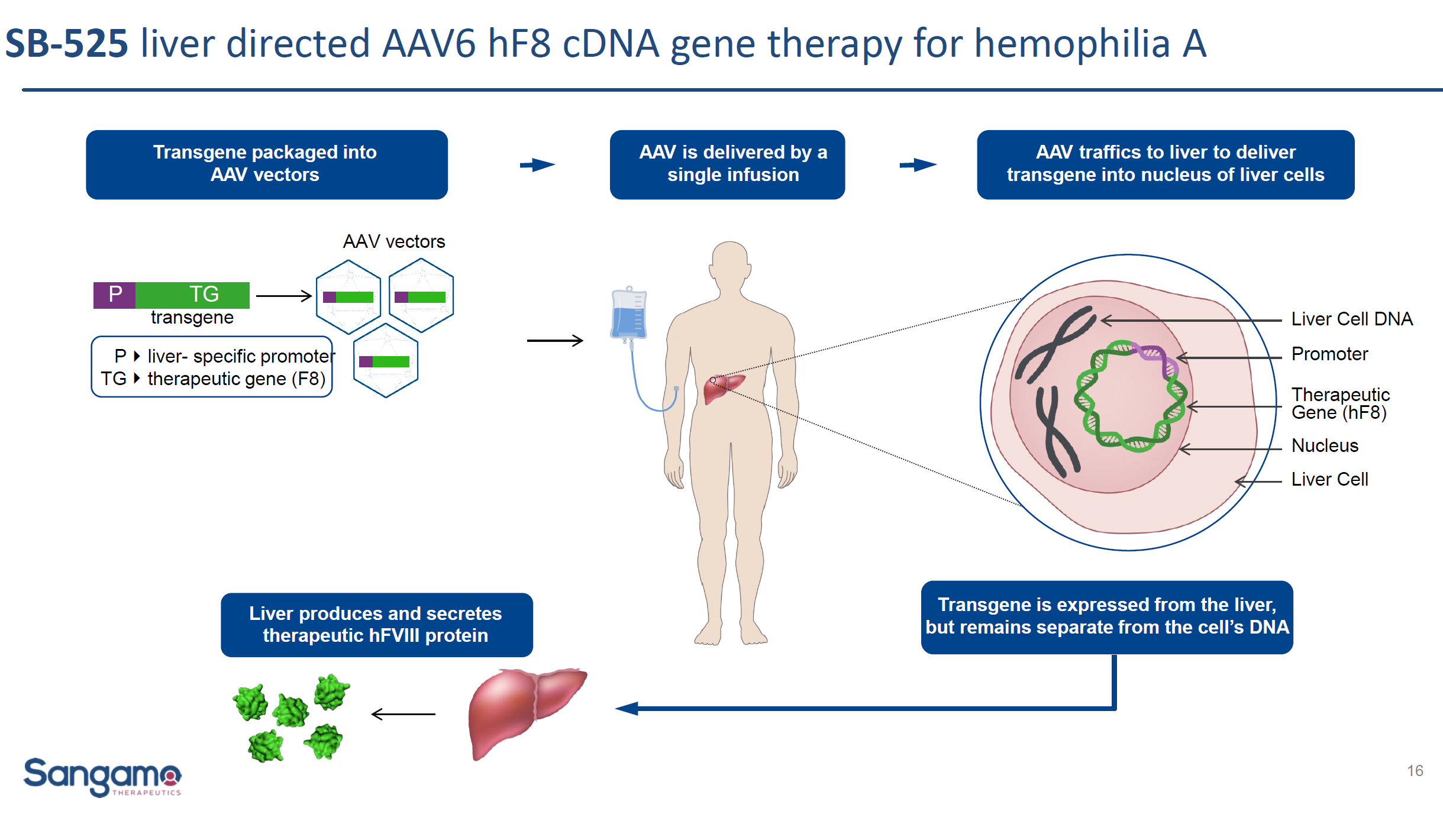
2019年公布的数据显示,SB-525能够针对A型血友病患者快速起效。最初给予最高剂量SB-525的两名患者分别接受了19周和24周随访,患者凝血因子VIII的活性维持在正常水平。与此同时,两名新入组的患者的人凝血因子VIII水平也有所上升,其中一名患者在接受治疗7周后超过了正常水平,另一名患者也已经缓解到了轻度血友病的程度。
Sangamo在与Pfizer的合作中已经收到了针对SB-525的7000万美元预付款,此外还可能获得高达3亿美元的里程碑式付款,用于SB-525的开发和商业化。除此之外,该公司还将获得1.75亿美元的其他A型血友病相关产品的资金。
目前,Sangamo公司已经完成了SB-525向Pfizer的技术转移,后者接手下一阶段的研究工作。自2019年12月,Pfizer开始了为期6个月的III期临床试验(NCT03587116),从那时起,Pfizer需要消耗相当一段时间才能完成III期临床试验的注册研究。该试验目前正在全球65个地点招募约125名患者,预计将于2021年结束。

BMN270疗法是一种基于AAV2/5的基因治疗疗法,在肝脏特异性启动子的控制下,BMN270携带一个健康的凝血因子VIII基因拷贝。由于肝脏特异性启动子的存在,凝血因子VIII蛋白只能在肝细胞中产生。然后它被分泌到血液中。
针对BMN270,BioMarin公司近日更新发布临床I/II期试验的四年追踪数据,数据显示该药物在治疗开始四年后仍继续安全、有效地预防出血。此次披露的研究结果已提交给于6月14日至19日举行World Federation of Hemophilia (WFH) Virtual Summit会议。
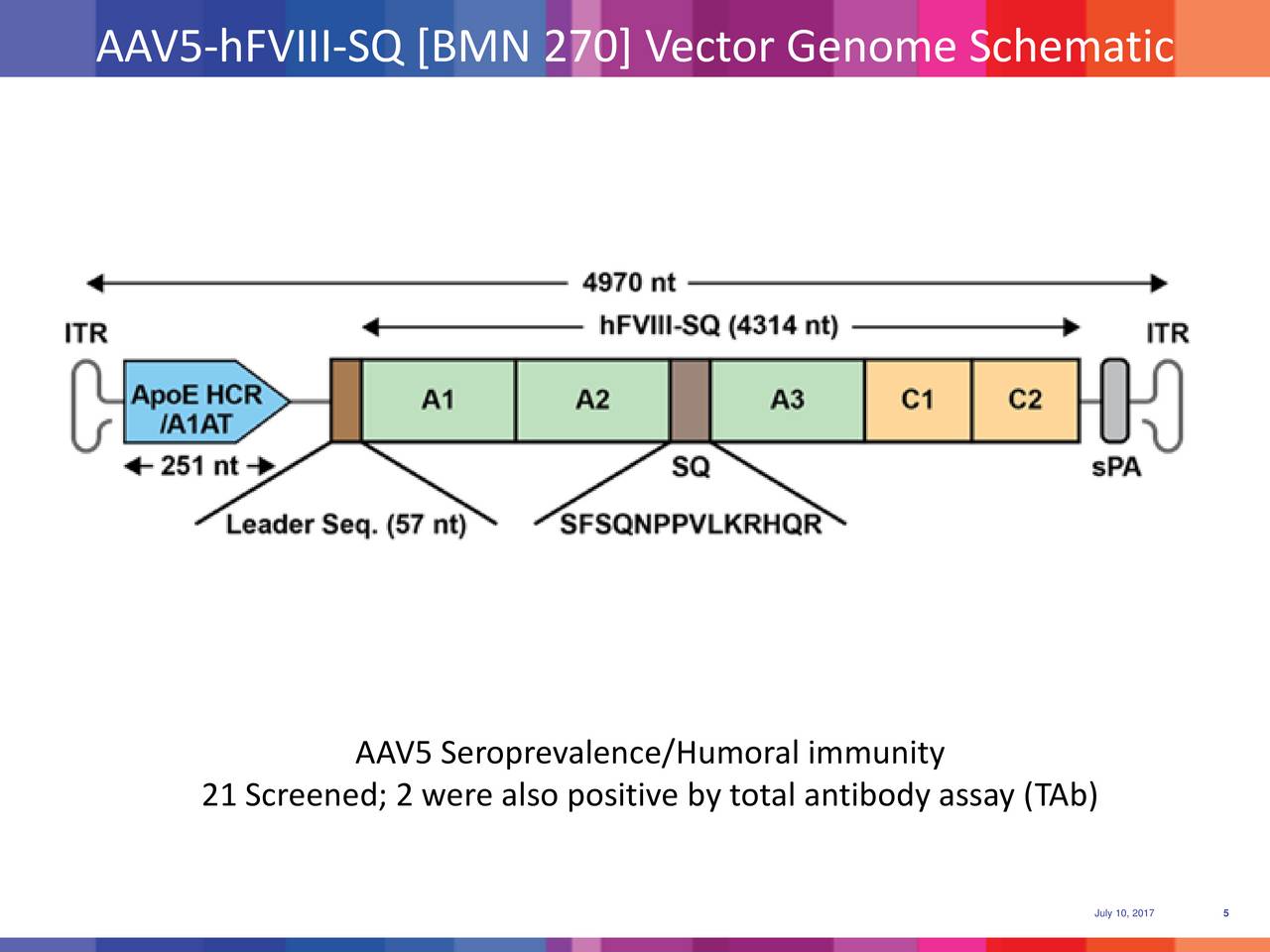
正在进行的I/II期临床试验(NCT02576795)正在评估四种不同剂量的BMN 270对15名患有严重A型血友病的成年男性5年内的安全性和有效性。
此前披露的三年数据显示,极低剂量组(AAV使用量:6*10^12和2*10^13vg/kg体重)的两位受试成年男性患者治疗三年后仍然有低水平的VIII因子,并仍在持续监测中。相比之下,其余受试的13位成年男性患者(6位给予4*10^13 vg/kg剂量,7名给予6*10^13 vg/kg剂量)显示凝血因子VIII的水平有临床意义的升高,平均年化出血率(ABR)显著下降,同时并不需要进行凝血因子VIII的辅助预防性治疗。
此次发布的数据包括6*10^13 vg/kg剂量组(高剂量组)的4年临床数据更新和4*10^13vg/kg剂量组(低剂量组)的3年临床数据更新。结果显示,所有受试患者均继续不需要接受凝血因子VIII的预防性治疗,他们的平均ABR仍维持在较低水平(高剂量组为1.3,低剂量组为0.5,明显低于治疗前的比率)。
在过去一年中,接受高剂量治疗的6名男子(86%)和接受低剂量治疗的5名男子(83%)均未发生出血事件。受试者的凝血因子VIII活性水平随年龄成比例下降,但仍继续处于治疗范围内。
BMN 270基因疗法目前正在接受美国FDA的优先审查,并接受欧洲药物管理局(EMA)的加速评估,以快速推进该药物的临床使用。如果获得批准,它将以Roctavian的品牌名称上市。
针对A型血友病,全球还有大量研发中的疗法尚未进入临床阶段或准备进入临床阶段,借助腺相关病毒载体在肝脏表达凝血因子VIII的疗法还将继续在基因治疗领域掀起热潮,我们期待此类疗法早日上市,让患者一针痊愈,让基因治疗造福人类。

和元生物基因和细胞治疗载体CDMO平台可提供从非注册临床研究用质粒和病毒生产(IIT)、基因治疗新药临床申报整体方案(IND)到基因治疗临床样品及商业化GMP生产的整体服务,服务产品包括基因和细胞治疗用质粒、腺相关病毒、慢病毒、腺病毒、多种溶瘤病毒以及基因疫苗等新型基因载体。
基于近4500m2的基因载体研发生产综合平台、近6000m2的基因载体GMP生产平台,以及2020年启动建设的逾8万平米和元智造精准医疗产业基地,和元将持续专注于基因治疗CDMO服务,助力基因治疗造福人类。


扫一扫,反馈当前页面
和元生物