
有“毒”?内毒素—rAAV载体的“毒”中“毒”

什么是内毒素?
内毒素(Endotoxin):又称脂多糖(Lipopolysaccharide, LPS),由脂质A、菌体特异性多糖和非特异性核心多糖三部分构成,是革兰氏阴性细菌细胞壁外壁的组成成分,单位EU/mL。内毒素对宿主是有毒性的,脂质A是内毒素的主要毒性组分。
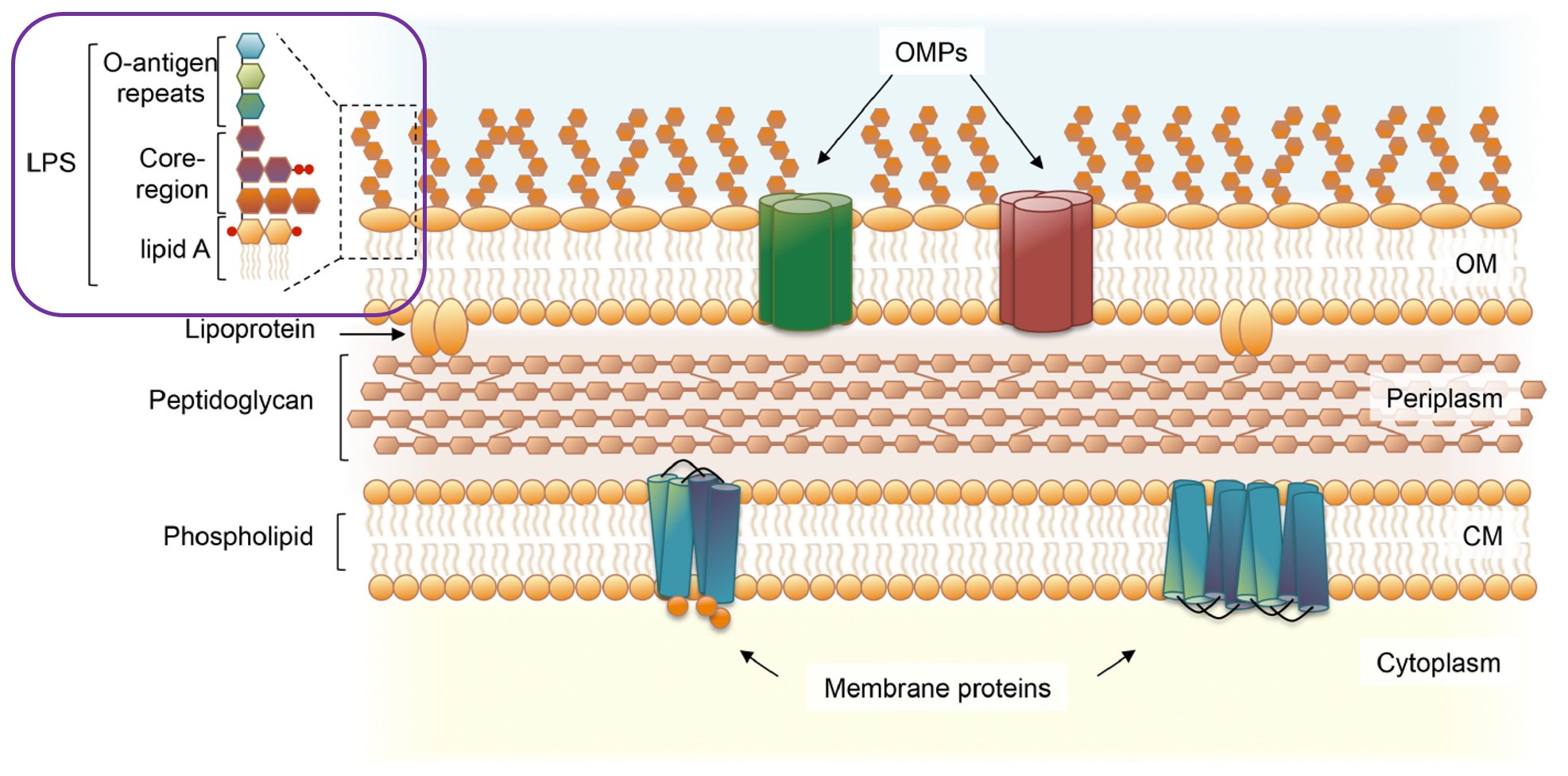
图1 内毒素分子结构(紫色方框所示,图片来源参考文献4)
rAAV载体中为什么会含有内毒素?
内毒素的释放是由细菌死亡自溶或粘附在其他细胞时造成的,也会发生在正常细胞生长和分裂过程中。在rAAV载体制备过程中,内毒素污染主要有两种来源:细菌内毒素和环境内毒素。由于rAAV生产所需要的质粒DNA是从大肠杆菌中分离提取的,因此质粒DNA可能含有少量内毒素;同时,rAAV制备过程中需转染293T细胞,而细胞的生长分裂可能也会带来内毒素的产生;此外,生产过程中的环境污染可能亦会引入内毒素。
rAAV载体中的内毒素如何检测?
根据药物生产的规范要求,基于鲎试剂的内毒素测定是检测内毒素残留的金标准。鲎是一种海洋节肢动物,身体呈青褐色,血液呈淡蓝色,鲎的血液一遇到细菌就会凝固。因此,人们利用这一特点开发出鲎试剂,即将鲎血液中的变形细胞进行溶解,将溶解物制成含有能被微量内毒素激活的凝固酶原产品,通过判断内毒素导致的浑浊效应测试内毒素含量。
通常,鲎试剂变性细胞溶液交联测定的敏感度是0.06个单位的内毒素EU/mL。测试样品用重蒸水两倍稀释使用,测定试剂(11uL)加入到rAAV溶液,培养在37℃,60min,试管检测胶块的出现,检测阳性和阴性结果。
内毒素对宿主的影响
内毒素对宿主是有毒性的,即使是少量的内毒素也可能会诱导宿主产生免疫反应。内毒素可以与细胞膜上的受体结合引起免疫反应,激活组织内的炎性细胞和炎症因子的释放,对细胞有较强的毒性作用,影响体内外细胞的生长和功能。在体内环境下,内毒素作用于哺乳动物,可导致机体发热,引发全身性炎症反应,继而引起弥散性血管内凝血、休克、多脏器功能衰减等,最终导致死亡。因此,无论是涉及病毒载体的实验研究还是临床应用,我们都需要尽量去除载体的内毒素。
如何有效去除rAAV载体中内毒素
在病毒的生产中,内毒素的去除包括亲和层析、缓冲液洗涤等方法,亲和层析法去除内毒素具有耗时、成本高、载体回收率差等缺点。缓冲液洗涤法则是借助超滤或离子交换色谱分离LPS胶束,经过多次缓冲液交换洗涤,再用低速离心浓缩病毒培养液的方式去除rAAV载体内毒素,该方法目前在部分rAAV血清型中适用。无论哪种方法都有一定的局限性,因此,从源头上去除内毒素至关重要。
基于12年、30000+的病毒生产经验,和元生物持续优化病毒生产全流程,建立标准三级细胞库,每月更换细胞,保证代次,持续降低rAAV载体的内毒素;同时,我们选择GMP级的质粒完成病毒包装,从源头上控制内毒素的产生。在实际工作中,多次、随机检测的rAAV载体内毒素含量均<2.5EU/ml,残留标准超出行业普遍的<10EU/ml,为研究者提供更好的基因载体,让基因递送触手可及。
别人只追求滴度时,我们还追求更有效;
别人只追求纯度时,我们还追求更安全;
别人只追求承诺时,我们还追求更真实;
别人只追求周期时,我们还追求更稳定。
在看不见的地方努力,
只为给您提供稳定的高品质产品!
和元生物用心做科研
让基因递送触手可及
业务咨询
和元生物具有丰富的rAAV包装经验,优化病毒生产全流程,制备的rAAV载体多次随机检测内毒素含量均<2.5EU/ml,超出行业标准,满足临床前和临床研究需求,如果您有相关业务需求可扫描下方二维码联系我们,我们将尽快与您联系!

参考文献
[1] Qingyun Zheng, et al., Low endotoxin E. coli strain-derived plasmids reduce rAAV vector-mediated immune responses both in vitro and in vivo. Mol Ther Methods Clin Dev. 2021 Jun 24;22:293-303.doi: 10.1016/j.omtm.2021.06.009.
[2]Liudmyla Kondratova, et al., Removal of Endotoxin from rAAV Samples Using a Simple Detergent-Based Protocol. Mol Ther Methods Clin Dev. 2019 Sep 6;15:112-119.doi: 10.1016/j.omtm.2019.08.013.
[3]Jihad El Andari, et al., Production, Processing, and Characterization of Synthetic AAV Gene Therapy Vectors. Biotechnol J. 2021 Jan;16(1):e2000025.doi: 10.1002/biot.202000025.
[4] Rita F Maldonado, et al., Lipopolysaccharide modification in Gram-negative bacteria during chronic infection. FEMS Microbiol Rev. 2016 Jul;40(4):480-93.doi: 10.1093/femsre/fuw007.

扫一扫,反馈当前页面
和元生物