
Mol Psychiatry. | 陆军军医大学牛建钦/肖岚团队联合揭示病理性少突胶质前体细胞参与精神分裂症的机制
精神分裂症(Schizophrenia)是一种复杂而严重的精神疾患,其特征是感知现实的方式受到严重损害,出现持续性妄想、幻想、思维混乱及行为异常等,影响到全球约2400万人。精神分裂症患者病理变化包括少突胶质细胞分化受损、髓鞘和白质丢失等。
精神分裂症断裂基因1(Disrupted-in-schizophrenia-1, DISC1)被认为是精神分裂症发病的主要易感基因之一,研究发现,DISC1功能障碍参与影响少突胶质细胞前体细胞(oligodendrocyte precursor cells, OPCs)的成熟和髓鞘的形成。此外,DISC1的部分致病单核苷酸突变将导致DISC1的可变剪切增加,其中DISC1-Δ3(缺少外显子3的剪切体)在精神分裂症患者中显著升高,但其致病机制仍不清楚。
2022年9月21日,陆军军医大学牛建钦教授团队联合肖岚教授团队、曼切斯特大学Alexei Verkhratsky教授团队合作在Molecular Psychiatry上发表了题为“Pathological oligodendrocyte precursor cells revealed in human schizophrenic brains and trigger schizophrenia-like behaviors and synaptic defects in genetic animal model”的研究论文,揭示了OPCs中DISC1-Δ3表达通过调控Wnt/β-catenin信号通路异常激活与其下游Wif1高表达,参与精神分裂症发病机制。该研究找到一个临床干预精神分裂症的分子靶点—Wif1,并提供了强有力的实验依据。

结果
精神分裂症患者OPCs形态异常
首先,研究人员基于临床样本率先发现,精神分裂症(Schizophrenia)患者海马、前额叶皮层和杏仁核中被NG2标记的少突胶质细胞前体细胞(oligodendrocyte precursor cells, OPCs)的数量无明显变化,而形态发生改变,表现为更为复杂的肥大形态(图1)。
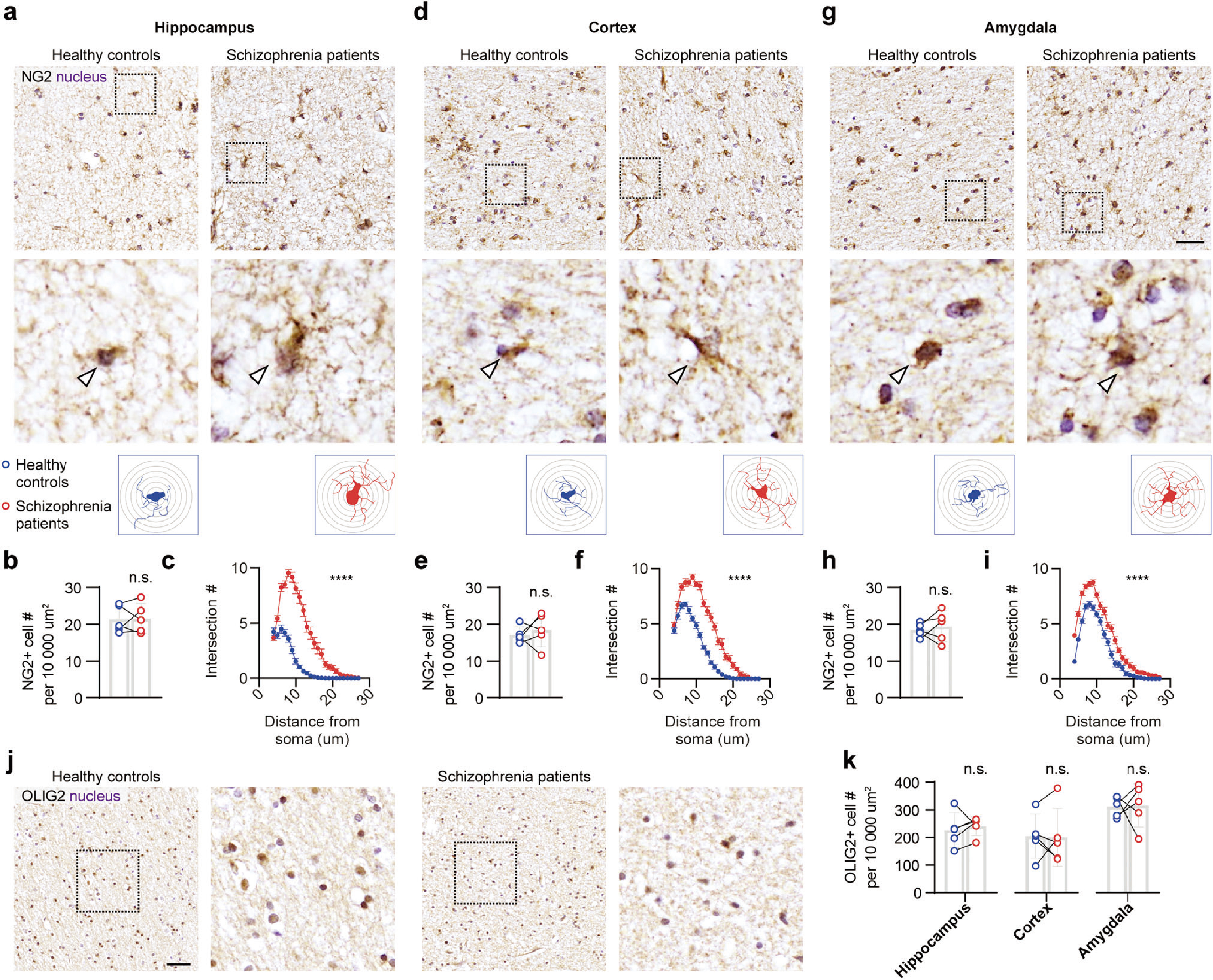
图1精神分裂症患者OPCs形态异常
DISC1-Δ3鼠模拟精神分裂症样表型
DISC1作为精神分裂症发病的主要易感基因之一,参与调节少突胶质细胞的发育,RNA测序结果显示,DISC1在人和小鼠OPCs的表达远高于少突胶质细胞和神经元。此外,对DISC1剪切体分析发现,DISC1-Δ3(缺少外显子3的剪切体)在精神分裂症患者脑中表达显著升高。 基于此,研究者构建NG2CreERT:DISC1exon3 fl/+小鼠(简称DISC1-Δ3鼠,由DISC1exon3 flox鼠与NG2CreERT鼠杂交获得,其特点为在不影响DISC1全基因表达情况下,经他莫昔芬诱导可特异性在OPCs中上调DISC1-Δ3的表达),发现OPCs中特异性过表达DISC1-Δ3同样导致OPCs过度肥大,并伴随着髓鞘形成减少(图2a-f),这与精神分裂症患者脑内OPCs形态类似(图1)。此外,行为水平上 ,出生后25-36(P25-P36)DISC1-Δ3鼠表现出精神分裂症样的感觉运动门控障碍(图2g-k)。同时,研究者发现DISC1-Δ3鼠海马CA1区兴奋性突触减少,且少突胶质细胞中DISC1-Δ3表达上调降低了自发兴奋性突触后电流(sEPSC)频率,增强了自发抑制性突触后电流(sIPSC)频率(图2l-p)。
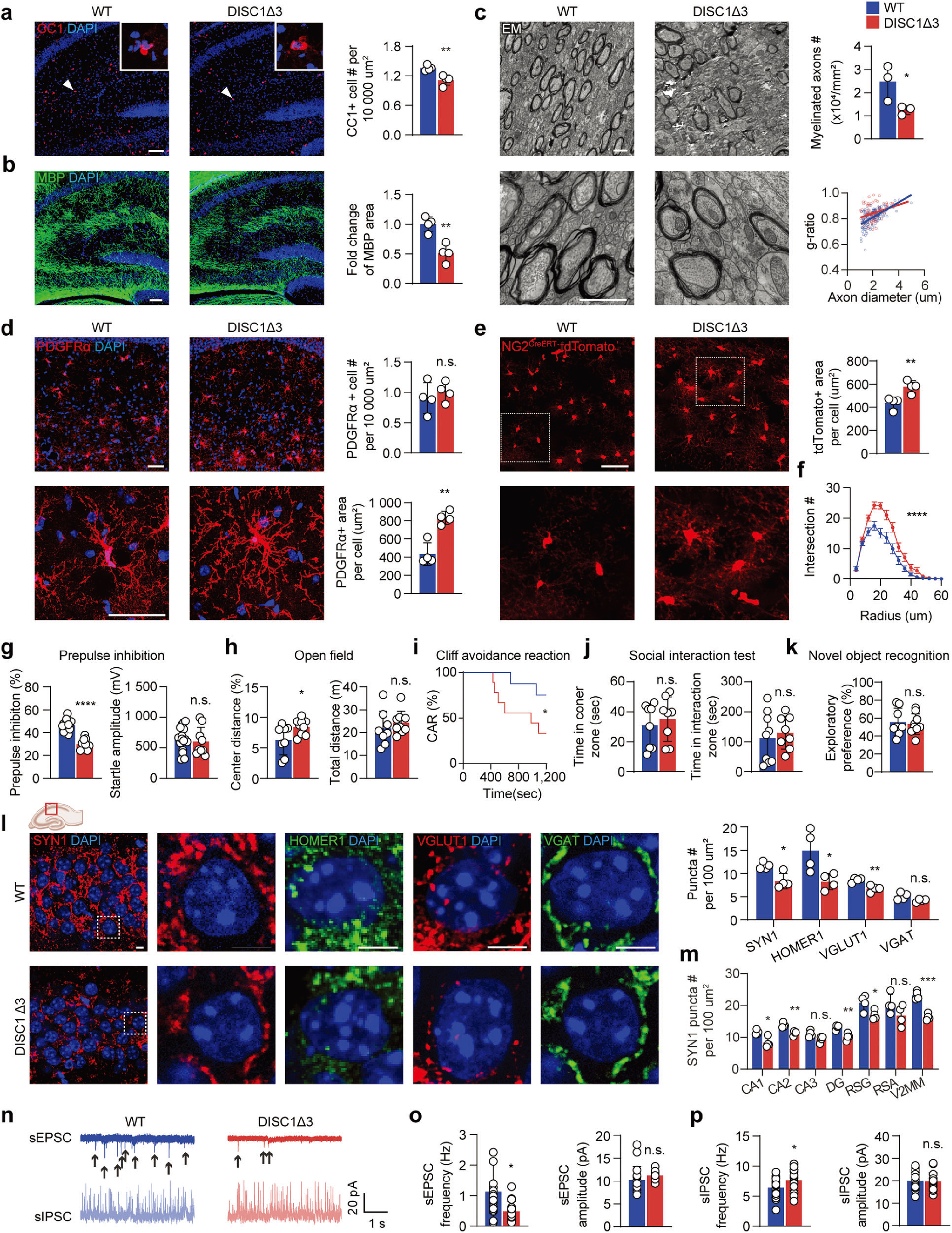
图2 DISC1-Δ3模型鼠模拟精神分裂症样表型
DISC1-Δ3模型鼠中OPCs异常参与突触形成缺陷及精神分裂症
随后,研究者分析了过度肥大的OPCs与精神分裂症患者髓鞘丢失的关系,通过他莫昔芬诱导DISC1-Δ3鼠在不同周龄发生OPCs中DISC1外显子3缺失,发现OPCs中DISC1外显子3缺失足以诱导突触功能障碍和精神分裂症样行为(图3a-f)。 接下来,研究者构建OL- DISC1-Δ3鼠(特异性在成熟少突胶质细胞中增强DISC1-Δ3表达)作进一步验证,发现特异性在P21小鼠海马OLs中增强DISC1-Δ3表达并未引起类似精神分裂症的病理变化(图3g-j)。同时,体外实验也验证了DISC1-Δ3 OPCs对神经元的直接影响(图3k-m)。 这些结果提示了,证明DISC1-Δ3小鼠中的突触形成缺陷与精神分裂症样表型是OPC本身的异常导致,而非髓鞘形成缺陷介导。
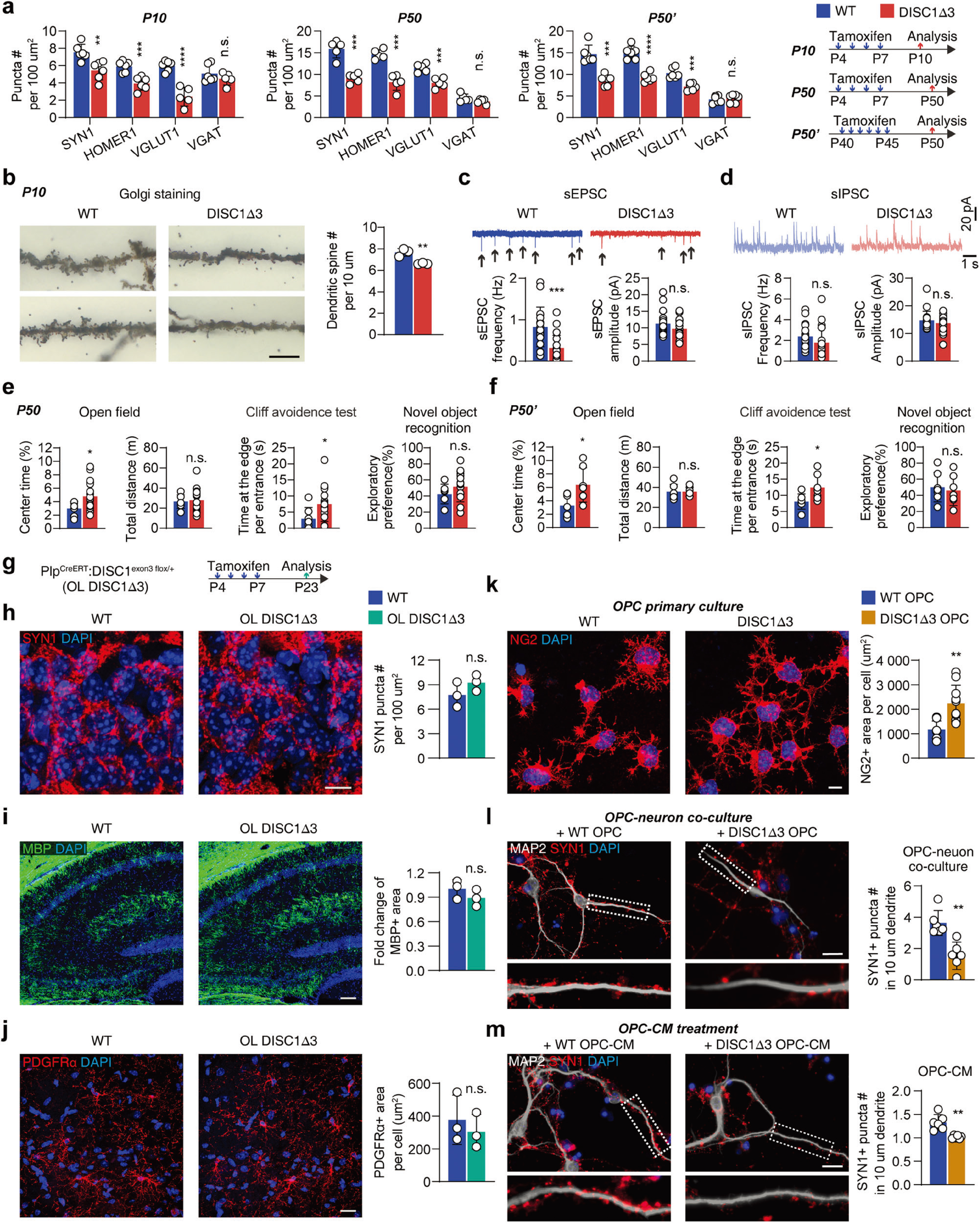
图3 DISC1-Δ3小鼠中的突触形成缺陷与精神分裂症样表型是OPC本身的异常导致,而非髓鞘形成缺陷介导
OPCs参与DISC1-Δ3模型鼠精神分裂症发生的分子机制
为验证其分子机制,研究者对急性分离的OPC进行RNA测序,发现在DISC1-Δ3 OPCs中Wnt/β-catenin信号通路过度激活(图4a,b),这是由于DISC1-Δ3通过Girdin-Akt通路间接抑制GSK3β活性,进而导致Wnt/β-catenin信号通路增加(图4a-d)。此外,基于临床样本,研究者发现精神分裂症患者海马区OPCs Wnt下游基因RNF43表达显著上调,这也印证了精神分裂症中少突胶质细胞前体细胞Wnt/β-catenin信号通路异常激活(图4e)。 接下来,研究者借助RNA-seq差异表达分析及分子生物学技术,在精神分裂症患者和DISC1-Δ3小鼠海马组织中发现Wif1表达显著增加(图4f-j)。并借助体外实验发现,Wnt/β-catenin过度激活的OPC通过Wif1抑制神经元中非经典Wnt通路,干扰突触形成(图4k,l)。
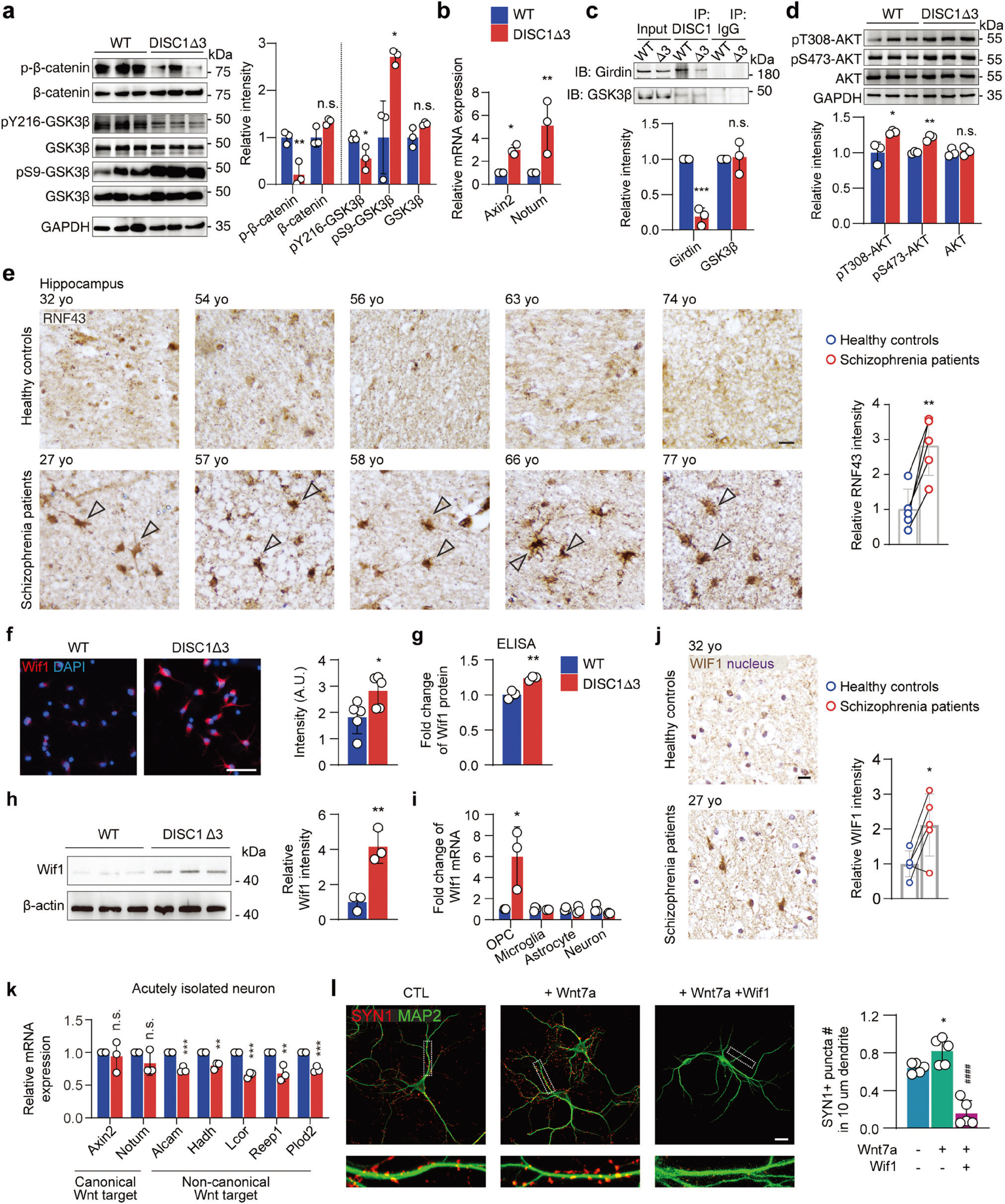
图4 DISC1-Δ3 OPCs中异常的Wnt/β-catenin异常激活
最后,研究者向P10 DISC1-Δ3鼠海马CA1注射逆转录病毒载体(特异性感染分裂期细胞)携带Wif1 shRNA(ROV-U6-shRNA(Wif1)-EF1A(S)-EGFP-3Flag)以特异性下调少突胶质细胞前体细胞中Wif1表达,发现增加了突触发生(图5a,b)。同样地,特异性敲除DISC1-Δ3鼠OPCs中Wif1,亦增强了海马兴奋性突触形成,并改善了精神分裂症样相关行为缺陷(图6c-i)。这些结果提示了,DISC1-Δ3鼠OPCs中Wnt信号通路异常激活通过调控Wnt抑制剂—Wif1表达量异常增加从而破坏突触形成,并启动精神分裂症的发病机制,下调OPCs中Wif1的表达可恢复DISC1-Δ3鼠突触形成,改善神经功能。
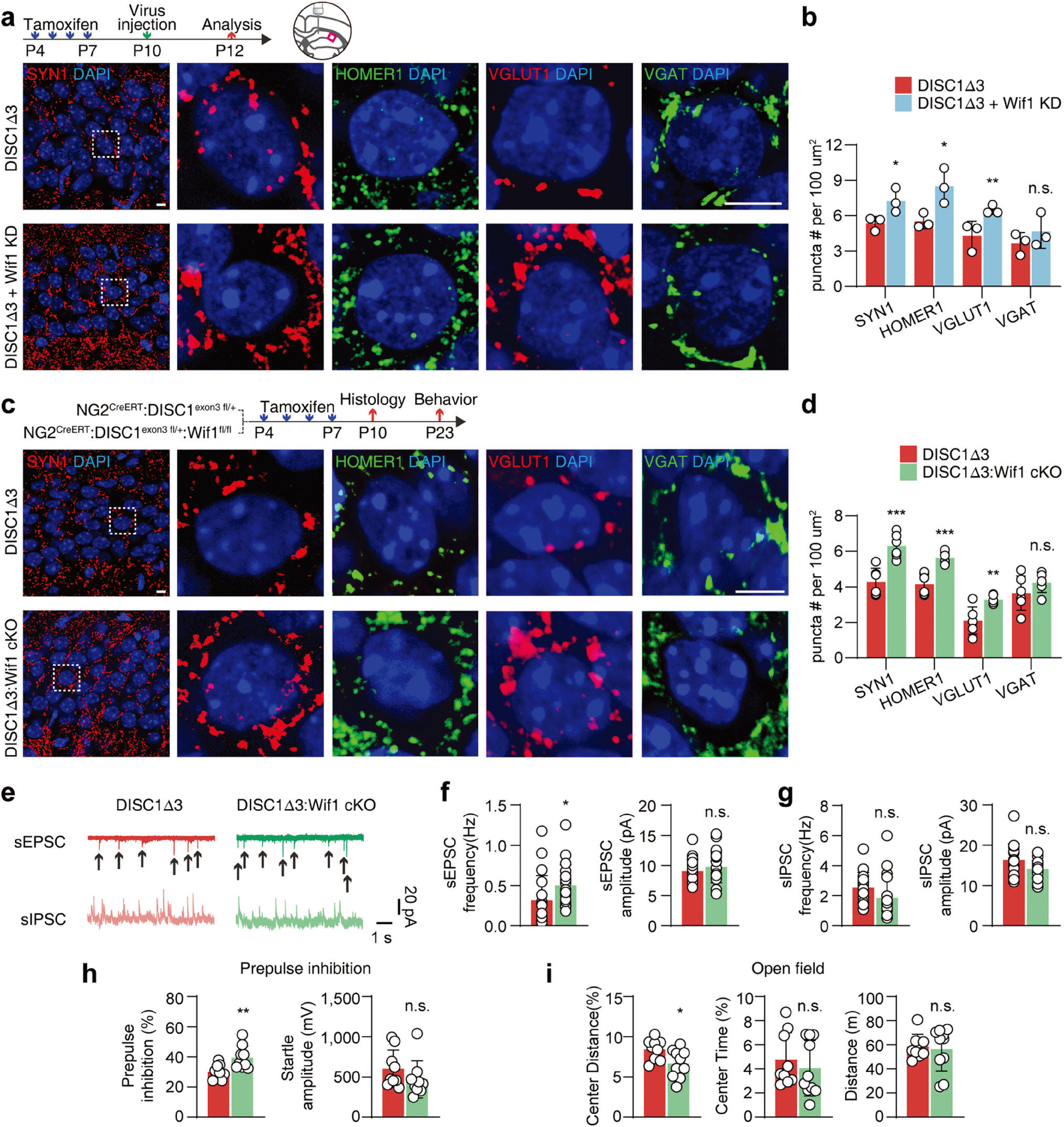
图5 下调OPCs中Wif1的表达可改善DISC1-Δ3鼠突触形成缺陷和行为障碍
结论

扫一扫,反馈当前页面
和元生物