
Nat Commun | 贵州医科大学郭兵等团队发现脂肪囊泡递送miR-30a-3p驱动肝脂质沉积,Sirt3作为上游“分子开关”
代谢功能障碍相关脂肪变性肝病(MASLD)是当前全球最常见的慢性肝病之一,其核心特征是脂肪组织功能紊乱以及甘油三酯在肝脏中的异常积累。脂肪组织不仅是机体重要的能量储存器官,还可分泌游离脂肪酸、脂肪因子及多种炎症因子,使肝脏更易受到脂毒性损伤并诱发代谢异常。然而,脂肪组织如何通过“远程”器官间通讯影响肝脏脂质代谢,其具体分子机制仍不清楚,这也限制了 MASLD 干预策略的进一步发展。
小细胞外囊泡(small extracellular vesicles,sEVs)是脂肪组织与肝脏之间信息交流的重要载体,可转运蛋白质、小分子和微小RNA(miRNA)等生物活性物质,进而改变受体细胞的代谢状态。前期研究证实,Sirt3可激活自噬以促进脂肪细胞脂解,并保护肝细胞免受脂毒性损伤。然而,Sirt3在调控脂肪细胞-肝细胞交叉对话中的作用仍未完全阐明。
·研究结果·
·研究结论·
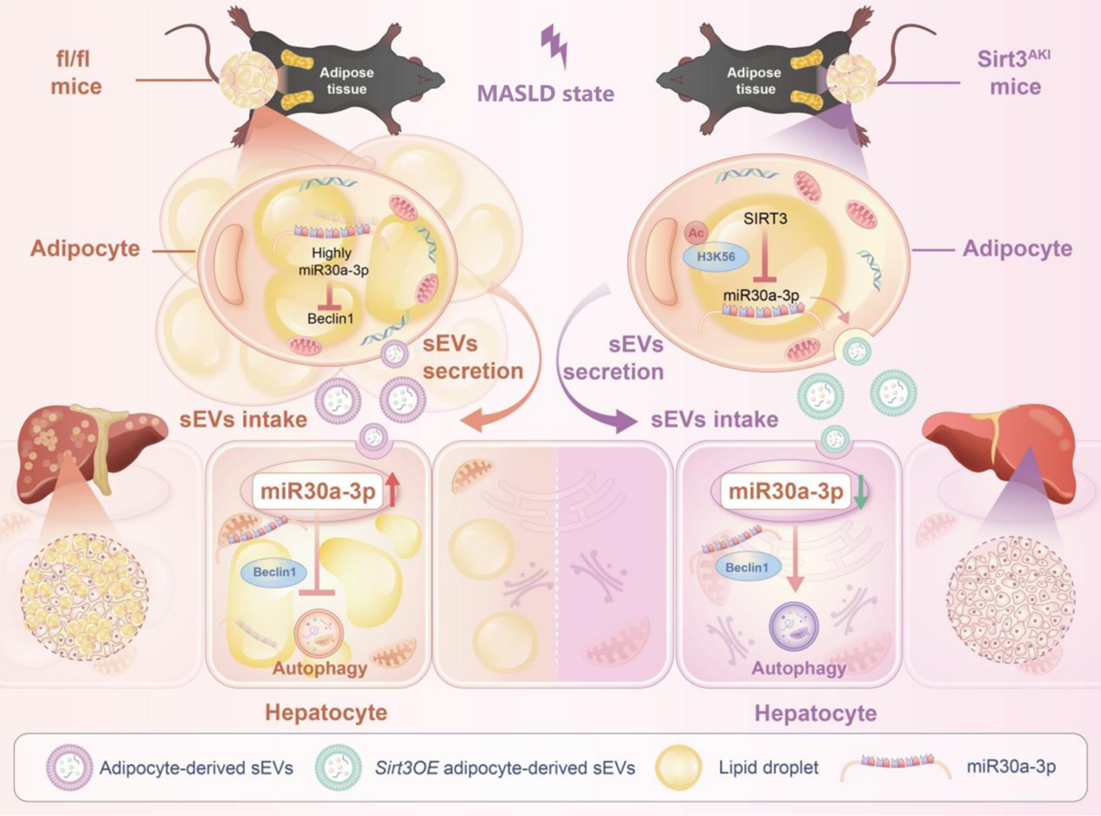
本研究首次阐明脂肪组织SIRT3去乙酰化H3K56 –miR-30a-3p–Beclin1信号轴,调控脂肪组织—肝脏器官间通讯,从而改善 MASLD 中的肝脏脂质沉积、胰岛素抵抗及肝功能损伤。不仅揭示了SIRT3在MASLD进展过程中的多器官交互中的作用机制,也提出了sEVs-miR-30a-3p可作为MASLD潜在的无创生物标志物与治疗靶点。
参考文献:
[1] Zhang T, Hu L, Chen D, Chen Y, Zhou F, Lou R, Zhou Y, Wang Y, Shi M, Linghu KG, Lin L, Guo B. Adipocyte small extracellular vesicle-derived microRNA-30a-3p exacerbates hepatic steatosis in high fat diet-fed male mice. Nat Commun. 2026 Apr 11. doi: 10.1038/s41467-026-71731-2
和元生物
和元生物成立于2013年,作为深耕细胞和基因治疗核心领域的高新技术企业,专注于为细胞和基因治疗的基础研究提供基因治疗载体研制、基因功能研究、药物靶点及药效研究等CRO服务,可提供①组学服务:常规转录组、单细胞转录组、基因组、代谢组及蛋白组等。②载体构建和病毒包装:质粒、siRNA、腺相关病毒(AAV)、腺病毒(ADV)、慢病毒(LVV)、逆转录病毒(RV)、单纯疱疹病毒(HSV)等病毒载体生产服务,提供R&D、实验室级别、GMP级别满足研发、小动物、大动物NHP到临床的不同研究阶段的使用需求。③细胞实验服务:过表达、干扰稳定株构建,单克隆细胞株构建服务及细胞功能学、药效学实验服务。④动物实验及机制研究:神经、代谢、肿瘤动物模型、药效药代、病理切片及蛋白、核酸检测服务。⑤特色项目服务:CRISPR文库筛选服务,外泌体整体研究服务,AAV衣壳筛选服务、听力研究整体项目服务,满足客户定制化或一站式项目服务,助力基础科学研究,促进基础研究到临床转化应用,推动细胞和基因治疗行业发展。

扫一扫,反馈当前页面
和元生物